1. Das afirmações seguintes indique as verdadeiras e as falsas, corrigindo estas.
A- O impulso de uma força constante é uma grandeza vectorial, cuja direcção e sentido são os mesmos dessa força.
B- Numa colisão perfeitamente inelástica há conservação do momento linear e da energia cinética.
C- Um corpo animado de movimento circular uniforme tem velocidade constante e aceleração nula.
D- Desprezando a resistência do ar, pode afirmar-se que dois corpos de massas diferentes, largados da mesma altura, em queda livre, chegam ao solo com velocidades e momentos lineares iguais.
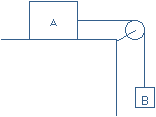
2. Considere o sistema representado na figura:

Suponha que a corda é inextensível e de massa desprezável. A intensidade da força de atrito entre o corpo A e a superfície em contacto é igual a 5,0 N. As massas dos corpos A e B são respectivamente 3,0 kg e 1,0 kg.
2.1. Faça o diagrama das forças que actuam no sistema.
2.2. Calcule:
2.2.1. o valor da aceleração do sistema;
2.2.2. a intensidade da tensão do fio.
g = 10,0 m s2
3. A velocidade de uma partícula, de massa 1,0 kg, que
se desloca com movimento rectilíneo, varia com o tempo de acordo
com o gráfico:
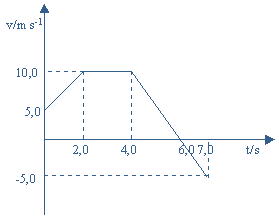
3.1. Complete as frases de forma a obter afirmações cientificamente correctas.
A- No intervalo [0 , 2,0[s, a partícula desloca-se com movimento rectilíneo ______ ______.
B- No intervalo [2,0 , 4,0[s, a partícula desloca-se com movimento ______ ______.
C- No intervalo [4,0 , 6,0[s, a partícula desloca-se com movimento rectilíneo ______ ______.
3.2. Para o intervalo de tempo [4,0 , 6,0[s, escreva a equação que traduz a lei:
3.2.1. das velocidades;
3.2.2. do movimento, considerando que a partícula no instante
t = 0 s se encontrava na posição 2,0 m.
Química
1. Na figura estão representados alguns níveis de energia
do electrão do átomo de hidrogénio.
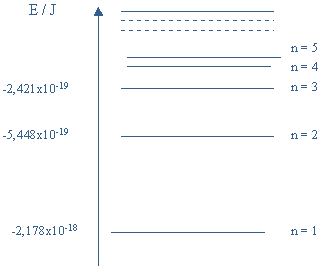
Calcule a energia da radiação de maior comprimento de onda que o electrão pode absorver quando se encontra no primeiro estado excitado.
2. Classifique como verdadeiras ou falsas as seguintes afirmações, corrigindo as falsas.
A- A frequência das radiações violetas é inferior à das radiações vermelhas.
B- Se um corpo opaco é azul é porque reflecte preferencialmente a cor azul.
C- A transição do electrão do átomo de hidrogénio de um nível superior para o nível 3 é acompanhada por absorção de uma radiação infravermelha.
3. Entre as seguintes proposições escolha as incorrectas.
A- A primeira energia de ionização do magnésio, 12Mg, é menor que a primeira energia de ionização do enxofre, 16S.
B- De dois iões isoelectrónicos monoatómicos, um positivo e outro negativo, o ião positivo tem maior raio.
C- Ao longo da Tabela Periódica, o raio atómico aumenta com o aumento do número atómico.
4. Considere as configurações electrónicas seguintes. A, B, C e D não são símbolos químicos de elementos.
A ![]()
B ![]()
C ![]()
D ![]()
4.1. Indique uma configuração electrónica impossível.
4.2. Localize na Tabela Periódica o elemento a que corresponde a configuração electrónica do átomo representada em A.
4.3. Indique uma configuração electrónica que diga respeito a um gás nobre.
5. Faça a correspondência correcta entre as duas colunas.
a- PH3 A- Molécula apolar com ligações polares.
b- CCl4 B- Molécula polar com ligações polares.
c- O2 C- Molécula com geometria angular.
d- NaCl D- Molécula com geometria tetraédrica.
e- K E- Molécula com geometria triangular plana.
F- Molécula com geometria piramidal trigonal.
G- Ligação metálica.
H- Ligação predominantemente iónica.
I- Ligação covalente dupla.
1H 6C 8O 11Na 15P 17Cl 19K
6. Indique o nome ou a fórmula de estrutura condensada, segundo a IUPAC, dos seguintes compostos.
A 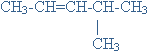
B ![]()
C ![]()
D ácido propanodióico
E 4- fenil-2-hexino
F metoxietano
7. Considere a reacção de oxidação-reduçãonuma
célula de níquel-cádmio traduzida pela equação
química:
![]()
7.1. Escreva as equações das semi-reacções que ocorrem no ânodo e no cátodo.
7.2. Indique a espécie redutora.