El ciclo de Carnot
Como,de acuerdo con lord Kelvin es imposible transformar en trabajo el calor que se toma de una unica fuente a temperatura uniforme mediante una transformacion que no produzca ningun otro cambio en los sistemas que intervienen en ella,para realizarla necesitamos por lo menos dos fuentes a dos temperaturas distintas,t1 y t2. Si contamos con dichas fuentes,podemos transformar el calor en trabajo por medio del proceso siguiente,denominado ciclo de Carnot.
Consideremos un fluido cuyo estado
pueda representarse sobre un diagrama (V,p),(volumen,presion) y
estudiemos dos ransformaciones adiabaticas(se dice
que una transformacion de un sistema termodinamico es adiabatica si es
reversible y si el sistema esta termicamente aislado de tal modo que no pueda
haber intercambio de calor entre el y el medio circundante mientras se
realiza la trasformacion) y dos transformations isotermas,correspondientes a las temperaturas t1
y t2(es la
transformacion durante la cual la temperatura del sistema permanence constante).
Estas
cuatro curvas se interceptan en los puntos A,B,C y D,como se muestra en la
siguiente figura,
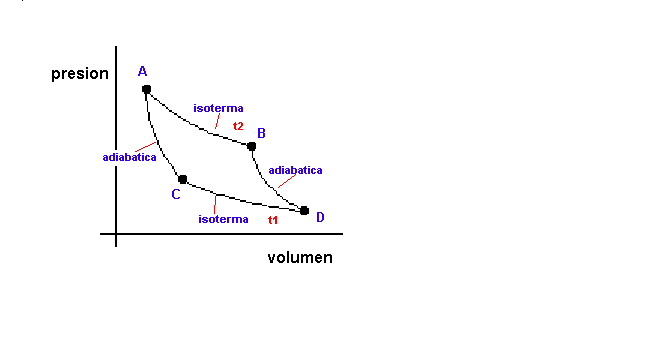
Sean AB y CD las isotermas de temperaturas t2 y t1
respectivamente.AC Y BD son las adiabaticas.La transformacion ciclica
reversible ABDCA,es lo que llamamos un ciclo de Carnot(se dice que una transformacion es reversible cuando los
sucesivos estados de la transformacion difieren de los estados de equilibrio en
cantidades infinitesimales,una transformacion reversible se realiza en la
practica variando muy lentamente las condiciones externas para asi permitir que
el sistema se ajuste gradualmente a las nuevas condiciones .Por ejemplo,podemos
producir una expancion reversible en un gas encerrandolo dentro de un cilindro
con un embolo movil y desplazando este hacia afuera muy lentamente.Si lo
desplazamos bruscamente se formarian corrientes en la masa gaseosa en expansion
y los estados intermedios dejarian de ser estados de equilibrio).
El siguiente ejemplo ilustra como se puede
realizar en la practica un ciclo de Carnot.
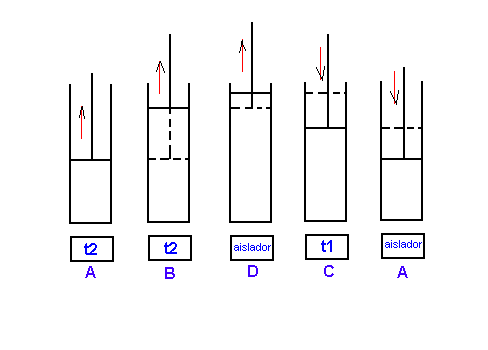
Encerramos
nuestro fluido en un recipiente cilindrico de paredes laterals no conductoras y
provisto de un embolo no conductor en un extremo,de manera que el calor solo
pueda salir o entrar en el cilindro a traves del otro extremo (la base) que
tomamos como conductora del calor.Sean t1 y t2 dos Fuentes de calor
suficientemente extensas de modo que su temperatura no sufra una alteracion
sensible si les agregamos o quitamos cualquier cantidad finita de calor.
Sea t2 mayor que
t1;suponemos que el volumen y la presion del fluido en el cilindro son
inicialmente VA y pA respectivamente,correspondiendo en el diagrama (V,p)
al punto A.Como este punto esta sobre la isoterma correspondiente a la
temperatura t2
,la temperatura del fluido es
inicialmente igual a t2 .Por lo tanto,si colocamos
el cilindro sobre la fuente t2 ,no se
producira transferencia de calor,punto A.
Manteniendo el
recipiente sobre la fuente t2 ,levantamos el
piston muy lentamente incrementado asi el volumen en forma reversible hasta que
hallamos alcanzado el valor VB ,punto B
.Esta parte de la transformacion esta representada por el segmento AB de
la isoterma t2 ,el estado de nuestro sistema esta representado ahora por el punto B
.
Colocamos ahora
el cilindro sobre un aislador termico e incrementamos el volumen muy lentamente
hasta que alcanza el valor VD
,punto D.Como durante el proceso
el sistema esta termicamente aislado,se representa con el segmento de
adiabatica BD.Durante esta expancion adiabatica ,la temperatura del
fluido decrece de t2 a t1, y el estado del sistema esta dado ahora por el punto D.
Poniendo el
cilindro sobre la fuente t1,comprimimos
ahora el fluido muy lentamente a lo largo de la isoterma DC,hasta que el
volumen disminuye a VC,punto C.Por ultimo
colocamos nuevamente el cilindro sobre un ailador termico y comprimimos muy
lentamente el fluido en forma adiabatica a lo largo del segmento CA
hasta que su temperatura se eleva a t2 .El
sistema habra vuelto a su estado inicial,que esta dado por el punto A.
Mientras se efectua la expancion isotermica representada por le segmento AB,el sistema absorbe una cantidad de calor Q2 de la fuente t2.Durante la compresion isotermica representada por el segmento DC,el sistema absorbe una cantidad de calor –Q1 de la fuente t1,es decir entrega a la fuente t1 una cantidad de calor Q1.La cantidad de calor absorbido por el sistema durante el ciclo es Q2-Q1.
Sea L el trabajo realizado por le
sistema durante la transformacion.Esta trabajo es igual al area limitada por el
ciclo en el diagrama (V,p) ;la primera ley de la termodinamica para un
ciclo es,
L=Q2-Q1
Esta ecuacion expresa que solo parte del
calor que absorbe el sistema de la fuente de mayor temperatura se transforma en
trabajo mediante el ciclo de Carnot ;el resto de calor ,Q1,en vez de ser
transformado en trabajo,es entregado a la fuente que se halla a menor
temperatura.
Definimos la eficiencia del ciclo de
Carnot a la relacion
h = L/Q2 =(Q2-Q1)/Q2
entre el trabajo realizado por el ciclo y el calor absorbido de la fuente a mayor temperatura.
REFERENCIAS
La maquina termica
PROCESOS
TERMODINAMICOS , La termodinamica trata
fundamentalmente de las transformaciones del calor en trabajo mecanico y de las
transformaciones opuestas del trabajo mecanico en calor.
Eduardo Ghershman,24.8.2002 enlace a CIENCIA