CIENCIA
Fuego y agua.
Esta pagina es un relato sobre el descubrimiento del
agua ,la misma abarca desde las primitivas teorias de Tales,pasando por las
pioneras investigaciones de Black, Cavendish y Lavoisier hasta los tarbajos de Gay-Lussac,con notas
aclaratorias sobre los conocimientos
actuales sobre la reacciones quimicas .
Flogisto.
Conviene aclarar que los cientificos relatados en
este estudio, por ser pionero, carecía de los conocimientos actuales sobre la
reacciones quimicas, por lo que esta exposición está basada en la
interpretación posterior de los trabajos de los mismos y las notas nos ayudaran
al entendimiento del tema.
Durante unos dos mil anos,despues del nacimiento de la ciencia y de la filosofia occidentales en la antigua Grecia, con
la figura de Tales, el agua se acepto como elemento basico del universo.
El mismo Tales, la consideraba como el elemento basico a partir del cual
derivaban todas las cosas.
Empedocles, filosofo griego nacido un siglo
despues que Tales, modifico esta concepcion, postulando la existencia de cuatro
elementos basicos : fuego, aire, agua y tierra y dos fuerzas motrices:
amor y lucha. Todo lo existente, decia Empedocles;deriva de estos factores y
ellos permiten explicar todo lo que sucede en la Naturaleza.
Solo una vez
desarrollados los metodos del analisis quimico cualitativo y cuantitativo, en
el siglo XVIII, pudo demostrarse que ninguno de los "elementos" de
Empedocles era, en verdad, elemental, y que el fuego no podia calificarse de
"sustancia".
Mas aun,el esfuerzo
por mantener la supuesta naturaleza del fuego ante la creciente acumulacion de
pruebas en contrario, fue lo que
incito los primeros y largos pasos hacia el descubrimiento del agua tal como
hoy la conocemos.
Desde epocas muy antiguas, se sabe que
algunas sustancias queman en el aire (son combustibles) y otras no (son
incombustibles). Menos evidente, pero al alcance de la observacion exacta, es
el hecho de que, entre las sustancias combustibles, algunas desaparecen de la
vista y del tacto cuando queman, dejando una ceniza de peso muy inferior
al de la sustancia original, mientras otras queman produciendo una ceniza mas
pesada que el cuerpo original. Esto ultimo se aplica, sobre todo, a las
sustancias metalicas: cuando se las somete a un calentamiento intenso, se
transforman en lo que durante el siglo XVII se llamo cales (hoy reconocemos en ellas a los
oxidos metalicos, cuyo peso es, a menudo, muy superior al que puede, a veces, invertirse,
quemando la cal (oxido de hierro, por ejemplo) mezclada con carbon de lena : en
este caso, la cal se transforma en el metal original y mas liviano, del
cual proviniera. Como explicarian en la antiguedad este fenomeno?
Nota: si realizamos en el
laboratorio la experiencia de obtener hierro a partir de su oxido,la ecuacion
siguiente lo explica en forma parcial :
Fe2 O3 + 3CO---------> 2Fe +
3CO2
El oxido ferrico se
combina con el oxido de carbono,dando dos moleculas de hierro y
tres moleculas de anhidrido carbonico,en este caso el peso del oxido ferrico es
superior al peso de las dos moleculas de hierro,en el siguiente dibujo el
lector puede ver como se deduce la reaccion(este dibujo debe ser entendido como
algo que nos permite llegar a la anterior ecuacion y es solo una ayuda):
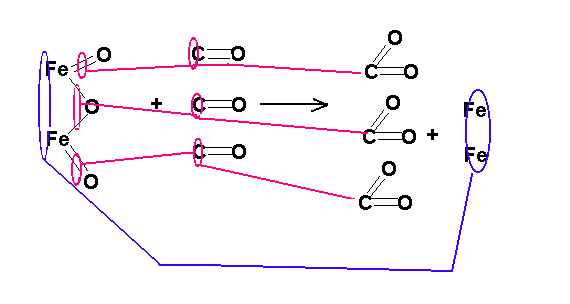
El carbono que actua con valencia 2 en el oxido de carbono, toma un oxigeno del oxido ferrico y pasa a tener valencia 4 en el anhidrido carbonico.
El quimico aleman G. E.
Stahl (1660-1734) ofrecio una explicacion parcial y en sus comienzos,
plausible. Stahl postulo la existencia de un "material y principio del
fuego'', al que diferenciodel "fuego mismo", y que llamo flogisto.
El carbon de lena, suponia,
era flogisto casi puro: cuando se calentaban cales en presencia de ese
carbon, ellas absorbian flogisto; durante la calcinacion (formacion de cales)
de los metales, se eliminaba flogisto. Stathl no presto atencion a los cambios
de peso producidos durante la combustion, mas sus sucesores inmediatos debieron
hacer frente a este hecho.
La solucion dada por estos
discipulos consistio en dotar al flogisto de una propiedad verdaderamente
notable: segun la nueva hipotesis, el flogisto poseia "peso
negativo". En otras palabras, se doto al flogisto de lo opuesto al peso, una propiedad de levedad o
ligereza. (Como las llamas siempre tienden a elevarse, los antiguos griegos
habian atribuido esta misma cualidad al fuego.) Asi, cuando se agregaba
flogisto a una sustancia, esta perdia peso y si se le extraia, el peso de la
sustancia aumentaba Esta teoria, absurda como parece a la mentalidad moderna,
se mantuvo, sin embargo, durante una centuria, como postulado basico y casi
universalmente aceptado de la quimica. Y no todos sus efectos sobre el
desarrollo de la ciencia fueron perjudiciales. La busqueda del misterioso
principio igneo de Stahl estimulo el desarrollo de aparatos y tecnicas de
laboratorio de creciente exactitud, muchas de los cuales forman parte del
analisis cualitativo y cuantitativo en la actualidad. Tambien estimulo
experimentos y explicaciones teoricas de sus resultados, todo lo cual abrio el
camino a nuestro actual conocimiento de que es el agua y por que se comporta
como lo hace.
El flogisto, por ejemplo,
ponia de manifiesto sus sorprendentes propiedades solo en presencia del
aire. No se formaba una cal si el metal se calentaba en el vacio. Por que
sucedia esto? El interrogante indujo a varias mentalidades de primera linea a
concentrar su atencion en el aire como tema de estudio cientifico, y
pronto realizaron experimentos mediante los cuales se descubrio que este
elemento, uno de los cuatro postulados por Empedocles, no era simple,
sino altamente complejo.
A menudo ,mas aun, en su
mayor parte, los experimentos no se concentraban directamente sobre la cuestion
que dejamos expresada mas arriba. El mencionado Joseph Black no le prestaba
atencion cuando, a mediados del siglo XVIII y siendo estudiante de medicina en
Glasgow, Escocia, realizo una serie de experimentos de suma importancia con
"tierras calcinosas" (caliza).
Si nuestra, pregunta anterior no hubiera despertado el interes por el aire, sin
embargo, quiza Black no habria parado mientes en el tipo particular
de "aire" que burbujeaba a traves del acido que habia vertido
sobre trozos de tiza. Asi las cosas, Black ideo experimentos para medir
las cantidades y propiedades de ese "aire", descubriendo que: a) no
mantenia la combustion (nada quemaha. en presencia exclusiva de ese gas); b)
aparecia en pequenas cantidades como constituyente del aire
atmosferico y podia separarse de este haciendo burbujear aire a traves
de agua de cal, formando, entonces, un precipitado de tiza en ese
agua; c) era un producto de la fermentacion de la cerveza, d) era
un producto de la combustion del carbon de lena y e) los pulmones
humanos lo emitian durante la respiracion.Black denomino a este gas "aire fijo”;hoy sabemos que se trataba del anhidrido
carbonico.
Nota :la caliza o piedra
caliza es el mineral del carbonato de calcio ,los minerales son
cuerpos inorganicos(solidos,liquidos o gaseosos),naturales,de composicion
quimica definida y de estructura homogenea,el carbonato de calcio CO3Ca ,se disocia dando oxido de calcio CaO (cal viva) y CO2 anhidrido carbonico,se descompone
por la accion de los acidos por ejemplo,con el acido clorhidrico ClH,descompone al
carbonato de calcio en agua,cloruro de calcio y anhidrido carbonico:
2ClH +CO3Ca------>H2O +Cl2Ca+CO2
A continuacion se dibuja
la obtencion de la anterior ecuacion (que el lector la debe tomar solo como ayuda
para escribir este tipo de ecuaciones) :
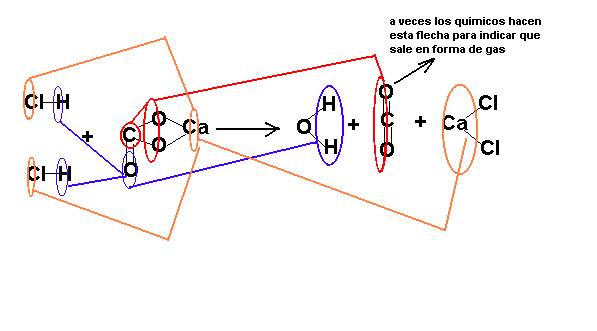
El gas
hidrogeno.
Poco tiempo despues, se
aislo otro gas importante. En realidad, la existencia de este gas habia sido demostrada
mucho antes de comenzar Black sus trabajos; mas aun, varios decenios antes de
que Stahl desarrollara la teoria del flogisto. Robert Boyle (1627-91), filsofo
ingles, generalmente considerado padre de la quimica, habia observado y
registrado que cuando se trataban limaduras de hierro con un acido mineral, se
producia la emision de un "aire" sumamente inflamable. Pero le cupo a
otro ingles, Henry Cavendish (1731-1810),que aplico, a mediados del
decenio 1760-70, metodos con los cuales obtener este "aire
inflamable" en forma pura, y con los cuales describir tambien sus
propiedades. Cavendish vertio acido sulfurico sobre trozos de cinc(o bien acido
clorhidrico sobre fragmentos de estano; el efecto es el mismo), recogiendo
el gas desprendido en un recipiente de vidrio, de forma cilindrica, lleno de
agua e inverlido de modo que su boca quedara dentro de una cubeta con agua.
Como el recipiente estaba lleno de agua, todo el aire habia side expulsado del
mismo. Cavendish hizo burbujear dentro de este el gas proveniente del cinc y el
acido, recogiendo asi una muestra en forma pura. En presencia del aire, esta
muestra resulto ser tan violentamente combustible que Cavendish, comparandola
con el "aire fijo'' de Black y suponiendo que provenia del metal, la
identifico con el flogisto. Hoy sabemos que se trataba del gas hidrogeno. Cavendish anuncio, su
descubrimiento en 1766; unos cinco anos despues, un fisico frances llamado
Antoine Laurent Lavoisier (1743-1794) inicio un imponente estudio experimental de
la combustion y calcinacion(formacion de cales) de los metales.
Nota : se obtiene hidrogeno
descomponiendo los acido diluidos por los metales,a la temperatura ordinaria
,utilizando el siguiente aparato :

Igual que Cavendish,se introduce acido sulfurico diluido junto con
trozos de zinc,que descompone al acido como se muestra en la siguiente
ecuacion:
Zn +SO4H2------> SO4Zn
+H2
Estas
operaciones se efectuan a la temperatura ordinaria .El aparato consta de un
frasco de Woolf,de dos bocas .Por una de ellas se introduce un tubo largo de
embudo,el cual penetra hasta el fondo;en la otra abertura se sujeta el tubo de
desprendimiento.Se echa en el frasco unos pedazos de zinc y un poco de agua y
se adapta el tapon con los tubos.Por el embudo se va echando poco a poco el
acido;el hidrogeno se desprende,expulsando el aire del aparato;cuando todo el
aire ha salido,se recoge el hidrogeno en unas probetas colocadas en la cubeta
de agua.
La cal roja de mercurio y el oxigeno.
A Lavoisier le llamo la atencion el gran aumento de peso observado despues de la combustion de fosforo en aire y se nego a aceptar la explicacion de que tal aumento era resultado del desprendimiento de flogisto con su fantastico peso negativo. Lavoisier prefirio suponer y en realidad esto le parecia evidente que el fosforo aumentaba su peso porque tomaba algo del aire en el cual se lo calentaba.Que era este "algo''? En 1774 aparecio una clave, cuando un quimico frances llamado Bayen dio cuenta de los resultados de algunos experimentos con cal roja (oxido rojo) de mercurio. Este polvo rojo posee ciertas propiedades notables, y Bayen abservo una de ellas: calento la cal sola (es decir, sin mezclarla con carbon de lena) hasta una temperatura muy poco inferior al "calor rojo'", y descubrio que la sustancia emitia un gas y se recuperaba mercurio puro. El gas era "aire fijo", anuncio Bayen, al parecer despues de examinarlo de manera muy superficial, si acaso lo examino. Muy poco tiempo despues, Lavoisier comenzo a realizar experimentos con la cal roja del mercurio, pero a diferencia de Bayen, presto, suma atencion al gas desprendido. Fuera lo que fuese, vio inmediatamente que este "aire" no era "fijo". Una bujia colocada en"aire fijo" se apagaba enseguida; colocada en el "aire" proveniente de la cal roja, quemaba con mayor intensidad. Entre tanto, al otro lado del Canal de la Mancha, el quimico ingles Joseph Priestley (1733-1804) tambien llevaba a cabo experimentos con la cal roja del mercurio. Pocos meses despues del anuncio de Bayen, que quiza no conociera, y varies meses antes de comenzar Lavoisier sus trabajos con esta cal, Priestley coloco el polvo rojo en una retorta cerrada, lo calento con una lente e hizo burbujenr en agua el gas desprendido,tal como lo hiciera Cavendish al descubrir el aire inflamable”.
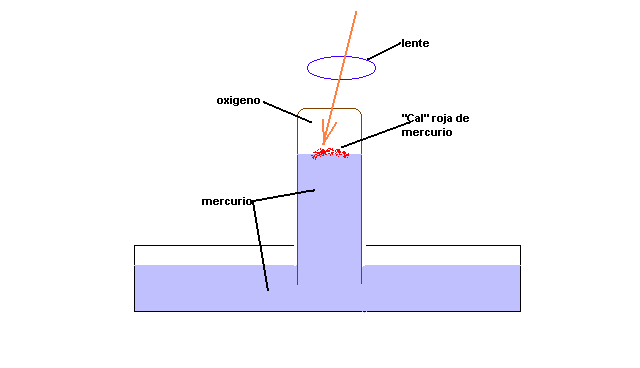
En el experimento de Priestley,este descompuso
la cal roja en mercurio y aire no “fijo”.Como el mismo Priestley escribiera en Experiments
and Observations(1775).”Pero,despues de procurarme una lente de doce
pulgadas de diametro y veinte pulgadas de distancia focal,me di a la tarea de
examinar con gran excitacion,con ayuda de la lente,que suerte de aire
suministraba una variedad de sustancias ,naturales y falaces,colocandolas en …
recipientes …, los cuales llene con mercurio y mantuve invertidos en un plato
del mismo material … ;el 1 de agosto de 1774 logre extraer el aire del mercurius
calcinatus per se y de
inmediato halle … “.Al parecer,Priestley no dejo dibujo alguno de su
aparato,pero la anterior figura ilustra el dispositivo usado.
Priestley tambien probo con una vela el “aire” asi
aislado,observando que era capaz de mantener la combustion y,por lo tanto,no
podia ser “aire fijo”(anhidrido carbonico).Podria,sin embargo ser “gas
hilarante” (oxido nitroso),cuyos extranos efectos sobre quienes lo inhalaban se
habian observado ampliamente,y asi lo supuso Priestley.
Abrigaba todavia esta opinion cuando dos meses mas
tarde viajo a Paris e informo a Lavoisier de su mas reciente
investigacion,estimulando a este ultimo a iniciar nuevos estudios en esta
linea. Es un
hecho historico, interesante por si mismo y representativo de la indole del
descubrimiento cientfico, que Bayen no fue el primero en observar que el
calentamieto de la cal roja del mercurio producia la emision de un gas y dejaba
como resultado mercurio puro. Lo mismo habia hecho en 1489 un alquimista
llamado De Sultzbach (llamo
"espiritu" al gas desprendido). Su observacion, sin embargo, no fue
sino otro hecho casual entre miles de observaciones
registradas por los alquimistas medievales en su busca de la "piedra
filosofal". Esta "piedra", como recordara el lector, era una
sustancia magica que permitiria al alquimista transmutar metales bajos, curar
todas las enfermedades humanas y lograr para si toda suerte de poderes
sobrenaturales. La observacion no comenzo a rendir frutos sino cuando el mismo
fenomeno fue observado por mentalidades disciplinadas con rigor y en
busca, no de poderes magicos, sino de verdades objetivas basadas en el razo
namiento causal.
Priestley era un habil tecnico de laboratorio y un observador
exacto, y ello le permitio llevar a cabo la labor basica. En
cuanto a Lavoisier, era no solo un tecnico de gran habilidad: estaba
tambien asombrosamente libre de prejuicios teoricos y podia concentrar en sus
observaciones una 1ogica de rara brillantez y una poderosa imaginacion creadora.
Constituye otro hecho interesante y significativo que ni Priestley ni Lavoisier
fueran los primeros en aislar y estudiar cientificamente el gas
obtenido de la cal del mercurio.
Nota : la cal roja de mercurio,es un solido en forma de laminillas
cristalinas de color rojo ladrillo,denominado oxido mercurioso,se obtiene
calentando mercurio a 350 grados Celsius de acuerdo a la siguiente ecuacion:
2Hg +O2 -------> 2HgO
se
puede realizar la operacion inversa,calentando el oxido mercurioso,se
descompone en mercurio y oxigeno.
El gran quimico sueco Karl Wilhelm Scheele (1742-1786) , aislo el gas
obtenido de la cal del mercurio en 1772 o 1773, dandole el nombre de
"aire igneo". Sin embargo, el manuscrito de su libro Aire y Fuego, con los primeros
informes sobre su trabajo, no fue enviado a la imprenta hasta 1775 y se publico
solo dos anos despues; los hombres de ciencia ingleses y franceses
desconocian por completo esas observaciones mientras realizaban sus
experimentos criticos.
En la ciencia es
importante contar con
comunicaciones rapidas y exactas. Los mismos impiden la repeticion innecesaria
de errores y aseguran la explotacion de los hechos descubiertos. La falta de
comunicacibn entre Scheele y sus colegas de otros paises le privo de su
merecida recompensa. Como consecuencia de ello, su obra tuvo un valor solo
marginal respecto de la corriente principal del progreso cientifico.
En cambio, entre Lavoisier
y Priestley hubo una comunicacion constante y de mutuo estimulo, mediante la
cual cada uno aprendio de los errores y tambien de los triunfos del otro. Asi,
por ejemplo, despues de su encuentro en Paris durante el mes de octubre de
1774, el ingles y el frances realizaron simultaneamente el mismo
experimento con el "aire" emitido por la cal de mercurio y
cometieron, al principio, el mismo error de interpretacion. Priestley lo
corrigio con rapidez, pero Lavoisier no lo hizo hasta que aquel se lo senalo,
mas el frances percibio idmediatamente el golpe mortal que ese
descubrimiento significaba para la teoria del flogisto, mientras que Priestley
se aferro a ella ,a la cual se hallaba, al parecer, ligado emocionalmente
durante toda su vida.
Temas relacionados:
IV. EN DONDE ARRECIAN LOS DESCUBRIMIENTOS DE SUSTANCIAS AERIFORMES
Y NO SE PERCIBE LO QUE SE TIENE BAJO LA NARIZ. Y EN DONDE SE VE QUE UN SIGLO
DESPUÉS DE LOS PRINCIPIA SE ENUNCIA UNA LEY FUNDAMENTAL Y NACE LA QUÍMICA
http://omega.ilce.edu.mx:3000/sites/ciencia/volumen3/ciencia3/118/htm/sec_7.htm
Eduardo
Ghershman,26.5.2001
enlace a CIENCIA