Установление механизмов реализации биологической активности отдельных аминокислот и их производных непосредственно связано с решением проблемы целенаправленной регуляции метаболического баланса.
В последнее время особый интерес исследователей привлекает естественный продукт превращений серусодержащих аминокислот таурин (2-аминоэтансульфоновая кислота), являющийся относительно незаменимым нутриентом с присущими ему радио-, гепато- и кардиопротекторными свойствами [3, 5-7, 9-13, 15,16,18]. По современным представлениям, биологическая роль этого соединения включает регуляцию окислительно-восстановительных реакций, ионных потоков и проницаемости клеточных мембран [4,14], а также процессов нейромодуляции в возбудимых тканях [1].
В многочисленных исследованиях продемонстрированы адаптивные сдвиги в обмене веществ при назначении фармакологически активных доз таурина [20-25], которые предполагают разработку лекарственных препаратов на его основе при заболеваниях центральной нервной системы [20]. Однако до сих пор остаются неисследованными регуляторные механизмы влияния таурина в концентрациях, сравнимых с эндогенными, на метаболические процессы, опосредующие реализацию его биологического действия. Доказательств прямой причастности таурина к многообразным физиологическим феноменам в возбудимых тканях, в которых таурин проявляет свойства нейромодулятора тормозного типа, более чем достаточно. Показано, что значительная часть нейрохимических эффектов аминокислот может быть реализована системными (энтеральным или парентеральным) способами их введения с одновременным воздействием на процессы формирования аминокислотного фонда в периферических тканях (печени, сердце, скелетных мышцах), характер которого необходимо учитывать при разработке способов целенаправленной коррекции метаболического баланса [2,8]. Однако, учитывая относительно плохую проницаемость таурина в мозг при периферических способах его введения (эффект повышения концентрации таурина в головном мозге в таких экспериментальных моделях достигался многократными инъекциями относительно больших доз препарата), для выяснения регуляторного действия эндогенных концентраций этого соединения оправдано субконъюнктивальное введение препарата: особенности кровоснабжения некоторых структур ЦНС, в частности, гипоталамуса, позволяют приравнивать такой способ к центральным (введение в желудочки мозга или спинномозговой канал) и обеспечить прямое поступление таурина в мозг. Целью настоящего исследования было выяснение возможности проникновения и избирательного накопления таурина в центральной нервной системе крыс при его субконъюнктивальном введении.
Животные
Крысам-самкам массой 140-160 г однократно вводили в конъюнктивальный мешок 14C-Tau (по 30 Ci на животное, в каждый глаз в объеме 10 л, без носителя). Крыс забивали декапитацией через 30, 60 мин, 2, 3, 6, 8, 24, 48, 72 и 120 ч после введения.
Забор материала для исследования
Крыс забивали декапитацией. Кровь (200 мкл) собирали в гепаринизированные пробирки и получали плазму центрифугированием на холоду. Образцы тканей забирали в течение 1 мин после забоя и фиксировали в жидком азоте. Головной мозг извлекали и препарировали гипоталамус на холоду [19]; пробы фиксировали в жидком азоте в течение 2 мин после забоя. Выбор данного объекта исследования обусловлен тем, что гипоталамус является структурой с наиболее высокой проницаемостью гематоэнцефалического барьера (что может означать высокую функциональную активность систем активного транспорта).
Оборудование и реактивы
В работе использовали: стандарты аминокислот, биогенных аминов и их метаболитов фирм Fluka, Serva, Sigma, Reanal; остальные реактивы - отечественного производства (квалификации не ниже хч) или фирмы "LaChema" (ЧСФР). Органические растворители имели квалификацию "осч для жидкостной хроматографии". Экстракционные среды и подвижные фазы, а также растворы стандартов готовили с использованием воды для ВЭЖХ, полученной тройной дистилляцией в стеклянном аппарате с последующим пропусканием через патрон "Norganic" и фильтрованием через мембранный фильтр HATF 0,45 мкм (Millipore, США).
Подсчет радиоактивности
В безбелковых экстрактах тканей головного мозга и гипоталамуса, а также плазмы крови, приготовленных так же, как для анализа свободных аминокислот, производили подсчет радиоактивности на жидкостном сцинцилляционном счетчике "Mark-II". Состав диоксанового сцинциллятора: 4 г/л PPO, 0,2 г/л POPOP, 10% метанола, 60 г/л нафталина, 20 мл/л этиленгликоля.
Математическая обработка результатов
Средние значения показателей в группах сравнивали
с помощью Т-критерия Стьюдента с использованием программам для медико-биологических
исследований из пакета ВМDР (BMDP Statistical Software) [17].
Сравнительно низкая проницаемость гематоэнцефалического барьера для таурина затрудняет воспроизведение его нейрохимических эффектов при периферических способах введения. Особенности кровоснабжения и проницаемости гематоэнцефалического барьера для гипоталамуса позволяют предполагать реализацию возможных нейрохимических эффектов таурина при субконъюнктивальном способе его введения и, возможно, приравнять его к центральным. В связи с тем, что для таурина не доказано наличие иных метаболических превращений, кроме конъюгации с желчными кислотами, мы исходили из предположения, что весь определяемый нами счет метки относится к таурину.
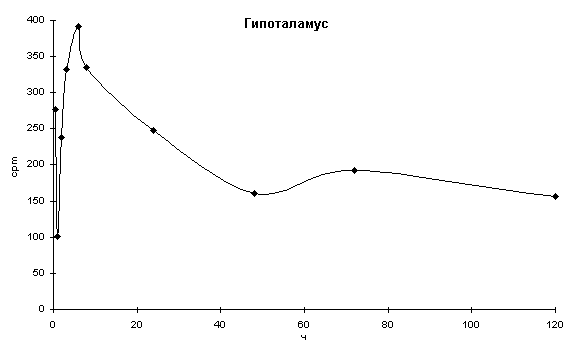
Результаты эксперимента по исследованию закономерностей распределения меченого 14C-таурина при его субконъюнктивальном введении животным свидетельствуют о наличии накопления метки в ткани гипоталамуса с максимумом через 6 ч после введения препарата (рис.1) и одновременным снижением уровня метки в плазме крови животных (рис 2).
На этом фоне кривая накопления 14C-таурина в целом мозге (рис.3) имеет вид, сходный с таковой для гипоталамуса, однако в мозге отмечается рост счёта метки вплоть до 5 сут эксперимента. Одновременно, кривая, отражающая закономерности накопления 14C-таурина для плазмы крови (рис.2) соответствует классической кривой элиминации, за исключением падения счета через 2 ч, после чего вновь наблюдалось увеличение счета (3 и 6 ч).
На основе полученных данных можно предположить существование процессов пассивной диффузии и активного транспорта таурина в гипоталамус при его субконъюнктивальном введении. Указанные процессы определяются особенностями кровоснабжения этого отдела, на что указывает высокий уровень накопления меченого 14C-таурина в гипоталамусе уже через 30 мин после введения метки (рис.1). Очевидно, что в дальнейшем (1-120 ч) таурин проникает в мозг только путём активного транспорта, что подтверждается характером элиминации метки из крови: наиболее интенсивное накопление метки в гипоталамусе (6 ч) по времени совпадает с резким снижением счёта в плазме крови, где эта кривая явно отклоняется от обычной экспоненциальной формы (рис.2).

Рис. 1. Накопление метки в ткани гипоталамуса после однократного субконъюнктивального введения 30 Сi 14C-таурина
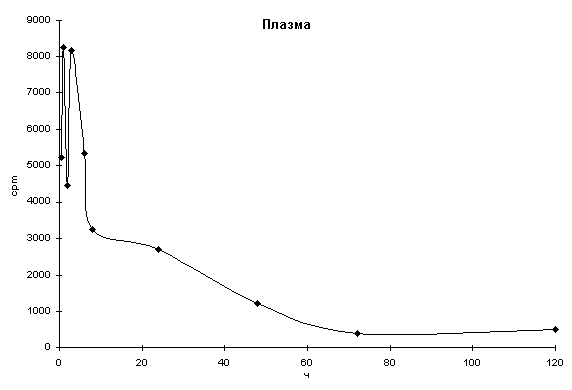
Рис. 2. Счет метки в плазме крови крыс через различные сроки после однократного субконъюнктивального введения 30Сi 14C-таурина.
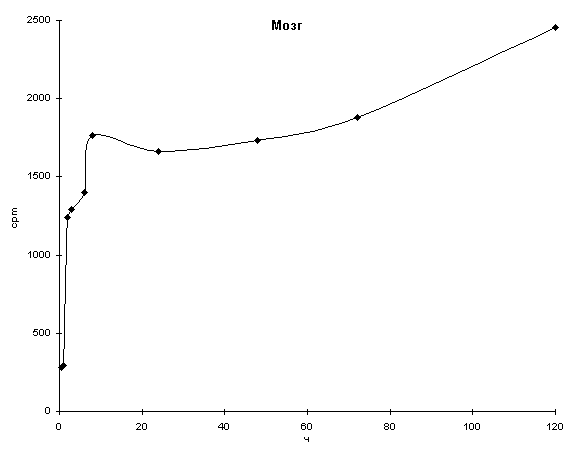
Рис. 3. Накопление метки в целом мозге крыс после однократного субконъюнктивального введения 30Сi 14C-таурина
Из полученных нами данных очевидно, что мозг имеет более чем одну систему активного транспорта таурина: с более низким сродством была активной и явно превалировала в гипоталамусе в ранние сроки (3 ч) от введения 14C-таурина, т.е. на фоне высокой концентрации метки в системном кровотоке; другая, очевидно, была ответственной за поздний (до 120 ч) подъём кривой в целом мозге и, таким образом, может быть преимущественно представлена в других структурах ЦНС. Кроме этого, в гипоталамусе имеется также пассивная диффузия таурина, чем объясняется проникновение метки в первые минуты после введения. В то же время, в гипоталамусе вплоть до конца эксперимента счёт метки оставался стабильно высоким с тенденцией к наличию второго максимума накопления - к 3 сут после введения.
Кинетические константы для таурина, рассчитанные из данных настоящего эксперимента, составили:
а) в гипоталамусе:
константа элиминации 0,01016 ± 0,00552 мин-1
период полувыведения Т1/2 68,22 мин
константа скорости всасывания Kt 0,72122 ± 0,37076
среднее время всасывания 1,38 мин
период полувсасывания 0,96 мин
максимальная концентрация 3,32 (cpm*1000)
б) в плазме крови:
период полувыведения Т1/2 13,88 час
константа элиминации 0,05 ± 0,026 мин-1
Таким образом, данные настоящего эксперимента подтверждают, что таурин является относительно долгоживущим соединением в ЦНС, и свидетельствуют, что:
1) субконъюнктивальное введение таурина позволяет получить его избирательное накопление в гипоталамусе за счет пассивной диффузии соединения, что можно объяснить особенностями кровообращения этого отдела мозга - наличием у гипоталамуса и тканей глазницы общих путей венозного оттока;
2) мозг располагает как минимум двумя системами активного транспорта таурина, причем одна из них вызывает раннее, т.е. в первые часы после введения таурина, проникновение соединения, и представлена в гипоталамических структурах;
3) эффекты таурина при его субконъюнктивальном
введении могут быть получены не только в гипоталамусе, но и в других структурах
ЦНС и могут иметь длительный характер.
Thus, taurine has relatively high half-life in the
CNS and its effects after subconjunctival administration might be obtained
not only in the hypothalamus but in other CNS structures and might be revatively
prolonged.