I. ВВЕДЕНИЕ
В многочисленной литературе имеется достаточное количество публикаций в области поиска и открытий новых лекарственных средств в качестве ингибиторов фибринолиза. Но только некоторые синтетические антифибринолитики нашли применение в клинической практике: е-аминокапроновая кислота (I), пара-аминометилбензойная (II) и транс-4-аминометилциклогексан-карбоновая кислоты (III). Идея использования синтетических ингибиторов фибринолиза возникла на основании биохимических исследований, установивших, что синтетические полипептиды из основных аминокислот угнетают фибринолиз. Однако, по оценкам некоторых исследователей, антифибринолитическое действие как полипептидов, так и отдельных аминокислот оказалось недостаточным для их практического использования. В частности, их применение не позволяет осуществить коррекцию системы гемостаза в фазе гипокоагуляции ДВС-синдрома [1], терапия которой является исключительно сложной задачей [2,3]. Поиск адекватных методов лечения ДВС-синдрома является весьма актуальным в связи с высокой частотой его развития у больных с сердечно-сосудистой патологией, в частности, при длительном лечении антикоагулянтами и дезагрегантами [4]. В этой связи нами и были проведены сравнительные испытания антифибринолитического действия широко известных синтетических ингибиторов I, II, III, L-лизина (IV), а так же проведен конформационный анализ ряда их аналогов - производных никотиновой кислоты. Для исследования механизма действия антифибринолитиков традиционно применяется ряд методов [2, 5,6,7], один из которых - метод фибриновых пластин достаточно прост, легко воспроизводим, дает высокую повторяемость, не требует сложной аппаратуры. Данный метод [8,9,10] базируется на необходимости расчета произвольных по форме площадей зон лизиса предварительно проинкубированных соединений. Традиционно применяемые аппроксимации площадей зон лизиса себя не оправдали [11,12,13] в оценке активности. Нами предложена компьютерная технология расчета площадей эллипсообразных фигур [14]. Путем варьирования времени преинкубации от 0 до 180 минут найдены оптимальные режимы для получения максимального эффекта в проведенных экспериментах.
Экспериментальные результаты анализировались методами многомерного статистического анализа и математического моделирования.
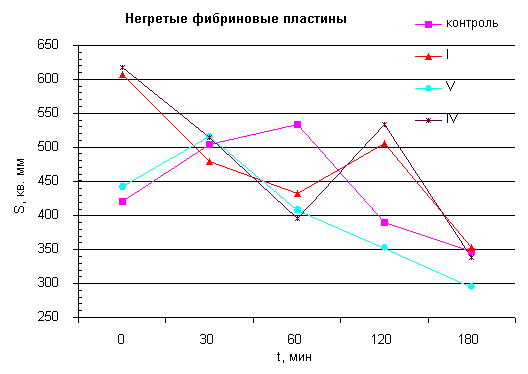
На рис.1 представлены результаты выбора оптимального режима преинкубации ряда исследуемых соединений: I, IV и V (никотиноил-е-аминокапроновая кислота).
Без предварительной преинкубации исследуемых соединений у I и IV получились соспоставимые результаты, у V - примерно на 5% менее. При 30 минутной преинкубации растворов происходят большие изменения у IV. При 60 минутной преинкубации - очень незначительные расхождения у I и IV, но более выраженная у V.

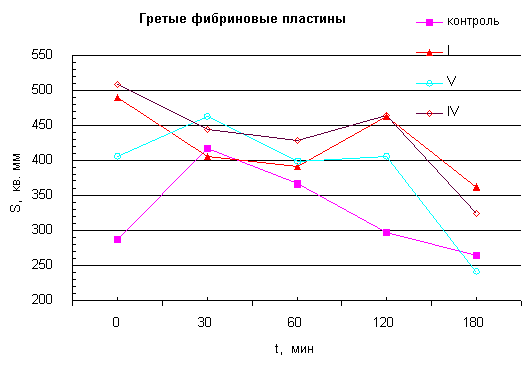
Рис.1
Табл. 1.
| Негретые пластины, S кв.мм | Гретые пластины, S кв.мм | |||||||
| t, мин | контр. | I | V | L-лизин (IV) | контр. | I | V | L-лизин (IV) |
| 0 | 420,8 | 606,7 | 442,4 | 617,1 | 287.2 | 490,1 | 404,9 | 508,4 |
| 30 | 504,2 | 478,8 | 516,4 | 513,8 | 416 | 405,5 | 462,2 | 444,4 |
| 60 | 532,7 | 433 | 407,3 | 396,7 | 365,8 | 390,8 | 397,3 | 428,2 |
| 120 | 390,1 | 505.5 | 351,6 | 533,3 | 297,1 | 461,9 | 404,5 | 464,3 |
| 180 | 347,8 | 353 | 294,2 | 338,5 | 264,3 | 361,8 | 240,7 | 324,5 |
В таблицах 2 и 3 представлены результаты влияния никотиноил-е-аминокапроновой (V), никотиноил-4-аминометилцикло-гексанкарбоновой (VI) и никотиноил-пара-аминометилбензоной (VII) кислот на плазминовую активность у белых крыс в условиях активирования системы фибринолиза, а также в опытах in vitro.
Результаты первой серии показали (см. табл. 2), что подкожное введение I, V-VII белым крысам, у которых путем введения тромбина был активирован фибринолиз, приводят к значительному снижению плазминовой активности плазмы крови.
При этом степень антиплазминовой активности у VI оказалась сравнительной с I, тогда как у V и VII была выражена ниже.
Результаты второй серии показали, что антиплазминовая активность исследуемых препаратов сохраняется в опытах in vitro, когда исследуемые вещества присутствуют в инкубационной среде в концентрации 10-2 М.
Табл. 2
| Статистические показатели | Группы | ||||
| контроль | I | V | VI | VП | |
| <Х> | 344.4 | 190.55 | 254.30 | 200.62 | 238.00 |
| S | 88.32 | 37.11 | 68.63 | 49-63 | 64-80 |
| PF1 | - | 0.97 | 0.53 | 0.85 | 0.63 |
| PF2 | - | - | 0.90 | 0.56 | 0.86 |
| PT1 | ~ | 0.99 | 0.97 | 0.99 | 0.99 |
| PT2 | „ | - | 0.97 | 0.36 | 0.93 |
| Доверит. интервалы для генеральных средних (р=0) |
|
]68.75; 218.79[ | ]33.00; 179.99[ |
| Статистические показатели | Группы | ||||
| контроль | I | V | VI | VII | |
| <Х> | 223.3750 | 110.25 | 106.8750 | 116.6250 | 129.6250 |
| S | 42.4464 | 31.6893 | 29.5898 | 32.8587 | 44.8169 |
| PF1 | - | 0.54 | 0.63 | 0.48 | 0.11 |
| PF2 | - | - | 0.13 | 0.07 | 0.61 |
| PT1 | - | 1.00 | 1.00 | 0.99 | 0.99 |
| PT2 | - | - | 0.17 | 0.30 | 0.66 |
| Доверит. интервалы для генеральных средних (р=0) | ]72.55; 153.69[ | ]65.64;
147.85[ |
]46.47; 141.02[. |
S - средняя квадратичная ошибка для одного измерения;
РF1 - вероятность принадлежности к разным генеральным совокупностям по отношению к контролю;
РF2 - вероятность принадлежности к разным генеральным совокупностям по отношению к I;
РT1 - вероятность различия центров распределения генеральных совокупностей по отношению к контролю;
PT2 - вероятность различия центров распределения генеральных совокупностей по отношению к I.
В табл. 3 представлены данные, отражающие специфическую плазминовую активность (за вычетом активности активаторов плазминогена) препарата плазмина Киевского завода бакпрепаратов в присутствии изучаемых веществ. Эти данные показывают, что в условиях непродолжительной (30 мин) преинкубации плазмина в присутствии изучаемых веществ наблюдается уменьшение последующего лизиса ФП. При этом препараты I, V и VI были практически одинаковы по степени антиплазминовой активности, тогда как действие VII было несколько меньше.
Была проведена сравнительная оценка L-лизина (IV) и I в качестве ингибиторов фибринолиза [15]. Структурный аналог IV - е-аминокапроновая кислота (I) широко применяется в хирургической практике в качестве ингибитора фибринолиза. Одновременно, IV присутствует как абсолютно незаменимая для организма человека аминокислота в большинстве искусственных аминокислотных смесей, применяемых при оперативном лечении широкого спектра патологических состояний, в количествах, сопоставимых с лечебной дозой I. Кроме того, IV рассматривается в настоящее время в качестве самостоятельного детоксицирующего средства, способного образовывать аддукты с низкомолекулярными соединениями (альдегиды и др.) при условии высоких концентраций этой аминокислоты в организме. Аминозоли и I назначается зачастую совместно без учета вероятной суммации антифибринолитического действия I и IV.
Нами на ФП модельных системах лизиса фибринового геля, инициированного стрептокиназой, проведено сравнительное исследование действия обоих соединений на систему активации плазминогена. Активность I и IV оценивали по полупериоду лизиса фибринового сгустка. Оказалось, что антиактиваторное действие обоих соединений на плазминоген учитывается при концентрациях IV > 10-2М, а I >10-4М.
Идея использования синтетических ингибиторов фибринолиза возникла на основании биохимических исследований, установивших, что синтетические полипептиды из основных аминокислот угнетают фибринолиз [16]. Однако антиплазминовое действие оказалось недостаточным для их практического использования. В этой связи были [17] произведены испытания с использованием результатов теоретического конформационного анализа в попарно-аддитивном приближении L-лизина и никотиноил-L-лизина (VIII) (вещество еще не синтезировано) с целью поиска потенциально более сильного лекарственного препарата-антифибринолитика. Отсчет углов вращения проводился по номенклатуре JUPAC/JUB, т.е. за нулевые значения углов внутреннего вращения принималась цис-конформация. Потенциалы невалентных взаимодействий рассматривались в форме 6-12 с параметрами В.Дашевского. Структура молекулы VIII приведена на рис. 2.
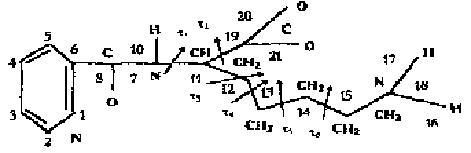
Рис. 2.
Установлен 21 центр взаимодействия у соединения VIII (ф1 -- .ф6). Фактически можно считать, что у молекулы VIII 6 углов (ф1 - ф6) внутреннего вращения. Авторы предполагают, что пока еще не синтезированное соединение VIII может явиться достаточно эффективным ингибитором фибринолиза.
Таким образом, нами показано, что соединения е-аминокапроновая кислота и L-лизин обладают сравнимой антиплазминовой активностью. Производные никотиновой кислоты проявили в целом более низкую антиплазминовую активность, за исключением никотиноил- е-аминокапроновой кислоты (V).
Однако вещество V, как легко детектируемое соединение, может использоваться для выяснения механизмов взаимодействия ингибиторов с компонентами системы плазмин. Предполагается, что соединение VIII окажется более выраженным анти-фибринолитиком, чем V, что позволяет рассматривать это соединение как более перспективное для разработки способов терапии ДВС-синдрома в фазе гипокоагуляции.
1. Лычев В.Г. Диагностические критерии ДВС-синдрома и их обоснование с помощью современных математических методов // Терапевтический архив.- 1986.- Т.58, №9.- С.124-129.
2. Павловский Д.П. Патогенез, диагностика и лечение синдрома ДВС: обзор литературы // Врачебное дело.- 1988.- №3.- С.73-77.
3. Климович И.И., Н.Н., Нефёдов Л.И., Дорошенко Е.М. Социальные факторы в профилактике и лечении атеросклероза: поиск новых препаратов для комплексной терапии на основе аминокислот // современные социально-экономические и правовые проблемы развития региона (тез.докл. межд. симпозиума). - Гродно, 1998.- С. 143-145.
4. Диссеминированное внутрисосудистое свертывание крови при ССП / Е.И.Соколов, И.В.Новикова, Т.П.Хованская и др. // Сов.медицина, 1987.- №3.- С.3-8.
5. Момот А.П. Разработка и клиническая апробация методов исследования производных фибриногена в плазме и сыворотке крови при ДВС-синдромах: автореф. дисс. … канд.мед.наук / Новосибирский мед.институт.- Новосибирск, 1990.- 17с.
6. Иванов Е.П., Цвирко Д.Г., Иванов В.Е. Методы определения плазминового фибринолиза крови // Здравоохранение Белоруссии.- 1990.- №2.- С.56-59.
7. Андреенко О.В., Карабасова М.А, Лютова Л. В. и др. Методы исследования фибринолитической системы крови. -М.:Изд-во МГУ, 1981.-131 с.
8. Буторов В. Н., Бокарев И. Н. Возможности метода фибриновых пластин для определения активности компонентов фибринолитической активности крови//Лаб. дело. -1978. -№5. -С. 271-273.
9. Astrup Т., Mullertz S. The fibrin plate method for estimating fibrinolytic activity//Arch Biochem. Biophys. -1952.-V. 40.-P. 346-351.
10. Bidwell E. Fibrinolysis of human plasma//Biochem. J. -1953. -V. 55. -P. 497-506.
11. Крашутский В.В. О новых принципах прогнозирования, диагностики, профилактики и лечения ДВС-синдрома // Воен.мед.журнал.- 1995.- №11.- С.12-23.
12. Н. Н., Клинцевич С. И. Компьютерная технология расчета площадей зон лизиса при определении фибринолитической активности/Гродно, 1991. -11 с. -деп. в ВИНИТИ 05.05.91, №1810-В91.
13. Н. Н., Бертель И. М., Клинцевич С. И. Компьютерная технология расчета методом Монте-Карло фибринолитической активности крови//тез. докл. IV съезда по клин. и лабор. диагн. Респ. Беларусь. -Гродно, 1992. -С. 143-144.
14. Клинцевич С. И., Н.Н. Математическая модель расчета площадей плоских фигур в медико-биологических экспериментах./ в кн.: Аладьев В.3., Сироджа И. Б., Байстрюченко Н.И.//Компьютерная смесь.-Таллинн, 1992- -С. 244-247.
15. Климович И. И., Клинцевич С. И., Н.Н. Сравнительная оценка L-лизина и е-аминокапроновой кислоты в качестве ингибиторов фибринолиза //Тез. докл. межд. научи, конф. -Гродно, 1993. -С. 415-416.
16. Влияние протаминсульфата на экспериментальный острый токсигенный ДВС-синдром / Г.А.Глазунова, З.С.Баркаган, А.П.Момот и др. // Гематология и трансфузиология.- 1988.- Т.33, №1.- С.22-28.
17. Н. Н., Голубович В. П. Расчет стабильных конформаций L-лизина и никотиноил-L-лизина//тез. докл. межд. симп. "Витамины и здоровье населения Беларуси и смежных регионов". -Гродно. 1995. -С. 206.
Key words: L-lysine, amino acids, nicotinoyl derivatives , mechanisms of action, fibrinolysis, plasmin activity, conformational properties of compounds, syndrome of long-term intravessel coagulation
New data has been obtained on the structural features of low-molecular-weight inhibitors of fibrinolysis and additional information - on the physico-chemical properties of the novel (not synthesized as yet) low-molecular-weight inhibitors of proteolysis of nicotinic acid derivatives, such as nicotinoyl-L-lysine. It has been shown that е-aminocaproic acid and L-lysine have a comparable antiplasmin activity. The nicotinic acid derivatives, with the exception of nicotinoyl-е-aminocaproic acid, manifested on the whole lower antiplasmin activity. As an easily detected compound, the latter can be used to elucidate the mechanisms of interaction of inhibitors with components of the plasmin system. It is suggested that nicotinoyl-L-lysine will exert a more pronounced antifibrinolytic effect as compared with nicotinoyl-е-aminocaproic acid, which will enable one to consider this compound as more promising for development of methods to treat the syndrome of long-term intravessel coagulation in the phase of hypocoagulation.
Mathematical models have been created,
numerical algorithms projected and programs elaborated for computer modelling
of the plasmin activity of L-lysine and other compounds. Programs have
been worked out for numerical experiments on the conformation properties
of pantoyl- and nicotinoyl-L-lysine with the help of current computer technologies.