УДК 577. 112. 387
В.Ю.Смирнов
1, Л.И.Нефёдов
1, Е.М.Дорошенко
1, И.И.Климович
2
Формирование
фонда свободных аминокислот и их производных в динамике введения таурина
1 Институт
биохимии НАН Беларуси,
2 Гродненский
Государственный медицинский институт
Принятые сокращения:
АРУЦ — аминокислоты с разветвленной углеводородной цепью; в/бр — внутрибрюшинное;
ЦНС — центральная нервная система; ЦТК — цикл трикарбоновых кислот; AST
— аспартат-аминотрансфераза (КФ 2.6.1.1); ALT — аланинаминотрансфераза
(КФ 2.6.1.2); b-Аlа — b-аланин; DA — 3,4-диоксифенилэтиламин (дофамин);
DOPAC — 3,4-ди-окси-фенилуксусная кислота; EA — этаноламин; GABA — g-аминомасляная
кислота; GDH — глутаматдегидрогеназа (КФ 1.4.1.2); 5-HIAA — 5-оксииндол-уксусная
кислота; 5-HT — 5-окситриптамин (серотонин); 5-HTP — 5-окси-L-триптофан;
HVA — 3-метокси-4-оксифенилуксусная (гомованилиновая) кислота; IDH — изоцитрат-дегидрогеназа
(КФ 1.1.1.42); LA — лактат; MDH — малатдегидрогеназа (КФ 1.1.1.37); 3-МТ
— 3-метокситирамин; PEA — фосфоэтаноламин; PDH — пируватдегидрогеназа (КФ.1.2.4.2.);
Таu — 2-аминоэтан-сульфоновая кислота (таурин); Trp — L-триптофан.
Таурин, конечный продукт превращений серусодержащих
аминокислот в организме, является относительно незаменимым нутриентам,
обладает радиопротекторным, антиоксидантным, мембраностабилизирующим действием,
является тормозным нейромодулятором, проявляет гепато- и кардиопротекторные,
антиаритмические и нормотензивные свойства [14,
20, 21].
Свойства этого соединения позволяют использовать лекарственные препараты
на его основе как эффективные средства при поражениях печени [18,
32, 33],
патологии сердечно-сосудистой системы [13,
27 - 29],
заболеваниях центральной нервной системы [8,
25], катарактах
и глаукоме, сахарном диабете, интоксикациях, а также наркоманиях и алкоголизме.
В настоящее время имеется большое число работ,
демонстрирующих широкий спектр эффектов фармакологически активных доз этого
соединения [2,
9, 11,
14, 17,
22 - 24,
31]. Однако, до
сих пор не исследованы регуляторные механизмы влияния таурина в концентрациях,
сравнимых с эндогенными, на метаболические процессы, опосредующие реализацию
его биологического действия, в частности, на процессы формирования фонда
свободных аминокислот и родственных соединений, на энергозависимые реакции
промежуточного обмена, обмен нейромедиаторов.
Продемонстрировано, что эндогенная концентрация
таурина является информативным показателем при патологических состояниях,
сопровождающихся развитием метаболического дисбаланса (как клинических,
так и воспроизведенных в эксперименте) [6].
На основании этого можно предположить, что ряд известных эффектов таурина
опосредуется влиянием на процессы синтеза de novo и деградации свободных
серусодержащих аминокислот, системы антиоксидантной защиты, функционирование
транспортных систем, а также патогенетически обосновать рациональность
его применения для коррекции метаболического дисбаланса.
Целью данного исследования являлось установление
закономерностей действия таурина в концентрациях, сравнимых с эндогенными,
на процессы формирования фонда свободных аминокислот и их производных в
ЦНС и периферических тканях.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В экспериментах использовались белые крысы-самцы
гетерогенной популяции массой 140-160 г, находящиеся на сбалансированном
рационе вивария. Изучение динамики воздействия таурина in vivo производилось
путем введения крысам в течение 15 суток Tau
внутрибрюшинно по 1/10 LD50 (650
мг/кг) в сутки в виде 4% раствора. Контрольные группы животных (для каждого
срока) получали соответствующий объем изотонического раствора NaCl. Забой
животных производился через 24 ч после последнего введения на 1, 3, 8 и
15 сутки эксперимента. Учитывая относительно плохую проницаемость Tau
в мозг при периферических способах его введения наряду с внутрибрюшинным
применялось субконъюнктивальное введение препарата: особенности кровоснабжения
некоторых структур ЦНС, в частности, гипоталамуса, позволяют приравнивать
этот способ к центральным, обеспечивающим прямое поступление Tau
в мозг, что было продемонстрировано нами в предварительных экспериментах
с введением 14С-Таu. Изучение динамики воздействия Tau
при его субконъюнктивальном введении производилось введением крысам Tau
в виде 4% раствора 4 раза в сутки по 10 мкл в каждый конъюнктивальный мешок
в течение 15 суток в суммарной дозе 1/10 LD50. Контрольные группы
животных получали воду аналогичным образом. Забой животных производился
на 1, 3, 8 и 15 сутки эксперимента через 12 ч после последнего введения.
Крыс забивали декапитацией. Кровь (200 мкл) собирали
в пробирки с 6% HClO4 для определения концентраций пирувата
и лактата; затем собирали в гепаринизированные пробирки и получали плазму
центрифугированием в течение 15 минут при 1500 об/мин на холоду. Образцы
периферических тканей (печени, скелетной мышцы, миокарда) забирали в течение
1 мин после забоя и фиксировали в жидком азоте, кроме этого, часть печени
помещалась на лед, для определения активности ферментов и содержания субстратов
в субклеточных фракциях. Головной мозг животных после забоя быстро извлекали
и препарировали отделы (гипоталамус, средний мозг и стриатум) при 4°С [19];
пробы фиксировали в жидком азоте в течение 2 мин после забоя; время до
фиксации каждого из отделов поддерживалось постоянным.
Экстракт плазмы крови для аминокислотного анализа
получали путем её депротеинизации 1M НСlО4 в соотношении 1:1
и центрифугированием в течение 15 минут при 8000 об/мин. Образцы печени,
сердца и мышечной ткани гомогенизировались при 800 об/мин в гомогенизаторе
со стеклянным пестиком в 10 объемах 0,2М HClO4, затем безбелковый
экстракт отделялся от осадка.
Определение концентрации свободных аминокислот
и их дериватов проводилось катионообменной хроматографией одноколоночным
методом на автоанализаторе аминокислот Т-339
[1]. Хроматографическое разделение исследуемых
соединений осуществлялось пятью Li-цитратными буферами на аналитической
колонке (22,0х0,35 см), заполненной сферическим катионообменником LGAN
2B (8 мкм). Количественное содержание исследуемых соединений определялось
фотометрически (при 520 нм) по реакции с 1% раствором нингидрина в капиллярной
бане при 100°С.
Определение уровней нейроактивных аминокислот
в отделах мозга проводили методом ВЭЖХ в хлорнокислых экстрактах. Образец
ткани гомогенизировали в 10 объемах 0,2 М HClO4, содержащей
внутренний стандарт - 2,5 мМ -аминовалериановую кислоту, а также 50 мг/л
ЭДТА и 50 мг/л Na2S2O5 в качестве антиоксиданта.
Свободные аминокислоты разделяли методом
обращенно-фазной хроматографии на колонке 3х150 мм, заполненной сорбентом
Диасорб-130 С16Т (8 мкм) с изократическим элюированием после
предколоночной дериватизации с офталевым альдегидом и 2-меркаптоэтанолом
и флуориметрическим детектированием (338/425нм). Концентрацию биогенных
аминов, их предшественников и метаболитов определяли методом ион-парной
ВЭЖХ на колонке Сепарон SGX C18 (5 мкм), 3х150 мм с предколонкой
3х50 мм; детектирование электрохимическое [3].
Митохондрии и гиалоплазму выделяли путем дифференциального
центрифугирования при 10000 g из 10% гомогенатов в среде выделения [5].
Активности AST
и ALT измеряли
по наработке пирувата, определяемой спектрофотометрически в реакции с 2,4динитрофенилгидразином
[10, 26]
Активность PDH
определяли по декарбоксилированию [1-14С]-пирувата, 14СО2
улавливали при помощи тиамин гидрохлорида, радиоактивность измеряли на
счетчике Mark II [16].
Активности MDH,
IDH и GDH
регистрировались спектрофотометрически по образованию или убыли восстановленных
форм никотинамидных коферментов [15].
Содержание пирувата и лактата определяли при помощи лактатдегидрогеназы
[7]; GL
- по наработке
NADPH в глюкозо-6-фосфатдегидрогеназой
реакции [4].
Хроматографические определения и отработку методов
проводили на хроматографе Waters (Waters Assoc., США) и автоматическом
хроматографе Т-339 (Чехия). Прием и обработка хроматографических данных
осуществлялась с помощью программно-аппаратного комплекса "МультиХром-1"
(Россия).
Для характеристики аминокислотного пула использовалась
Т-статистика и корреляционный анализ, реализоваными с помощью статистических
программ из пакета ВМDР (BMDP Statistical Software). Внутригрупповые значения
корреляций считали достоверными при значениях |r| = 0,78 и выше [12].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Ежедневное внутрибрюшинное введение Tau крысам
в дозе 1/10 LD50 вызвало на 1 сутки эксперимента снижение в
печени концентрации Gln и Lys и повышение уровней Ala и Tyr. Одновременно
происходило снижение активностей митохондриальной MDH и цитоплазматической
IDH и повышение уровня LA
(рис. 1). В плазме крови крыс отмечены менее выраженные сдвиги в содержании
исследуемых соединений - увеличилась лишь концентрация Ala. На 3 сутки
эксперимента в печени животных, получавших Tau, повысилась активность PDH,
увеличилась активность цитоплазматической MDH, а также сохранился повышенный
уровень LA (рис.
1). При этом в печени возникла положительная корреляцонная зависимость
между уровнем Tau и активностью цитоплазматической MDH. На этом фоне значительно
снижалась концентрация структурного аналога таурина - -Ala и возникали
высокодостоверные положительные корреляции между уровнем Tau и его структурного
аналога - PEA в печени, между Tau и Lys - в плазме крови и отрицательные
- между содержанием Tau и активностью ALT в плазме крови. Всё это, в сумме
с понижением уровня глюкозы на 8 сутки, может свидетельствовать об активации
процессов гликолиза в печени животных на фоне дополнительного введения
Tau. Характерно, что соотношение активностей митохондриальной и цитоплазматической
форм MDH снижалось на 1-3 сутки, что свидетельствует об ингибировании процессов
глюконеогенеза на ранних сроках внутрибрюшинного введения Tau [30].
Уровень Tau в печени и плазме крови повысился
только на 8 сутки эксперимента, что может объясняться насыщением систем
его конъюгации с желчными кислотами, в то время, как в более поздние сроки
могут включаться дополнительные адаптивные механизмы поддержания него концентрации.
Одновременно в плазме крови повысились концентрации незаменимых аминокислот
Thr и Lys. На 15 сутки в печени и плазме крови повысилась концентрация
Ala, что, учитывая снижение уровеня глюкозы в печени, свидетельствует об
активации процессов глюконеогенеза при длительном введении Tau.
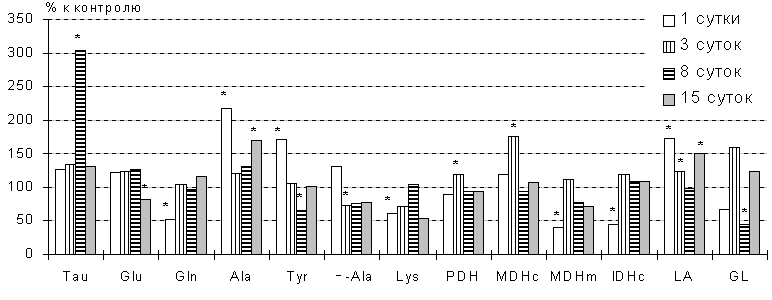
Рис. 1. Сдвиги концентраций
свободных аминокислот и их производных, лактата, активностей ферментов
цикла трикарбоновых кислот в печени крыс в динамике ежедневного в/бр введения
Tau в дозе 1/10 LD50. (Здесь и на рис.2-4: *
- p<0,05 по сравнению с контролем соответствующего
срока)
Обращает на себя внимание появление в печени
на 15 сутки эксперимента положительной корреляции в уровнях Tau и Met,
что может служить доказательством усиления синтеза эндогенного Tau при
его дополнительном введении в течении длительного срока, и появление отрицательной
корреляции в уровнях Tau и Ctn, что, вероятно, свидетельствует о уменьшении
относительной значимости других путей превращения Met. Так уменьшение скорости
образования Ctn может привести в свою очередь и к усилению относительной
значимости других путей превращения Ser. В пользу последнего предположения
говорит появление положительной корреляционной зависимости между уровнями
Tau и Gly, хотя повышение уровня последнего не было достоверным.
На фоне внутрибрюшинного введения Tau значительно
возросла его концентрация в скелетной мышце, особенно на 3 сутки эксперимента,
когда в опыте возникают высокодостоверные отрицательные корреляции между
уровнями Tau - Gly и Tau - -Ala.
Одновременно наблюдалось обеднение аминокислотного пула сердечной мышцы
(снижение концентраций Thr, Ala, Met, Leu, Lys) и, в меньшей степени, скелетной
мышцы, что не наблюдалось в более поздние сроки. К 15 суткам эксперимента
в скелетной мускулатуре на фоне высокого содержания Tau снижались концентрации
Gly, Asp и структурного аналога и транспортного антагониста Tau - -Ala.
К этому сроку опыта имеется тенденция к снижению содержания Tau в миокарде,
что подтверждает существование автономных систем транспорта и превращений
Tau в сердце.
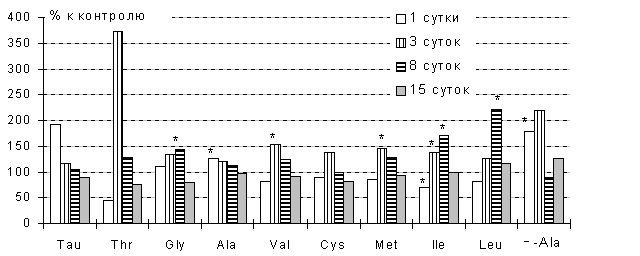
Рис. 2. Изменения уровней
свободных аминокислот и их производных в плазме крови крыс в динамике ежедневного
субконъюнктивального введения Tau в суммарной дозе 1/10 LD50
Концентрация Tau в печени и плазме крови при
его субконъюнктивальном введении не изменилась. На 1 сутки эксперимента
в печени увеличилось содержание LА, в плазме крови - Ala и -Ala и снизилось
- Ile. Наиболее выраженные изменения при этом способе введения в периферических
тканях отмечены к 3 и 8 суткам эксперимента и касаются, в первую очередь,
незаменимых и заменимых гликогенных аминокислот. В плазме крови на этих
сроках произошло обогащение фонда незаменимых аминокислот (Thr, Val и Ile),
увеличились концентрации серусодержащих аминокислот (Met и Cys), АРУЦ (Val,
Leu), а также дикарбоновых аминокислот (Gly, Glu) (рис. 2). Однако, на
15 сутки наблюдалась полная нормализация всего фонда свободных аминокислот
в плазме крови. Такая фазовость в изменениях уровней аминокислот вероятно
можно объяснить изменением процессов их деградации или распада белка В
печени опытных животных на 1 и 3 сутки возникли положительные корреляции
между уровнем Tau и уровнем его структурного аналога - PEA. В плазме крови
опытных животных при субконъюнктивальном способе введения концентрация
Tau коррелировала
с содержанием большинства гликогенных аминокислот. Уровни свободных аминокислот
в печени при этом значительно не менялись: на ранних сроках снизилось содержание
Phe, а на 15 сутки повысился уровень Leu, снизились активности ALT и цитоплазматической
IDH и уровень этаноламина. Субконъюнктивальное введение Tau незначительно
отразилось на структуре фонда свободных аминокислот в скелетной мускулатуре
- содержание Tau не изменилось практически на всех сроках, только на 3
сутки снизилось содержание Glu и на 8 - повысилось Gly. В сердечной мышце,
также, как и в скелетной, субконъюнктивальное введение Tau не изменило
его уровень и привело к увеличению на 1 сутки уровня Gly, на 3 сутки -
Asp, Thr, Cys и Orn. На 15 сутки эксперимента в этих структурах произошла
полная нормализация всего фонда аминокислот.
В целом мозге опытных животных внутрибрюшинное
введение Tau на ранних сроках (1 и 3 суток) от начала эксперимента увеличило
активность PDH и GDH, на 3 сутки снизило активность ALT и цитоплазматической
MDH. Cхожие изменения наблюдались после субконъюнктивального введения Tau:
на 1 сутки от начала эксперимента повысилась активность GDH, а на 15 сутки
- активность митохондриальной IDH, лимитирующей функциональную активность
ЦТК.
Уровень Tau при его ежедневном внутрибрюшинном
введении увеличивался в стриатуме и стволе мозга только на 15 сут, а в
гипоталамусе - начиная с 3 сут эксперимента. Через 1 сутки в стволе мозга
увеличивалось содержание Asp, Gly, -Ala и 5HIAA и снижалось - PEA; эти
изменения исчезали на 3 и 8 сут, а на 15 сутки снижалось содержание Trp
и Gly. В стриатуме через 1 сутки уменьшалось содержание PEA, через 8 суток
- DA и Gly, однако через 15 суток содержание DА и 3-МТ повышалось. В гипоталамусе
в сроках 1 и 15 сут снижалось содержание 5-НТР, на 1 сутки - Glu, на 3
сутки повышался уровень Gly и на 8 сут - Trp (рис. 3).
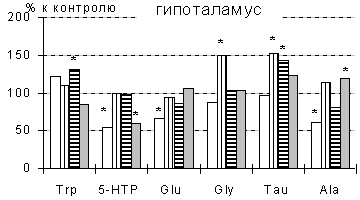
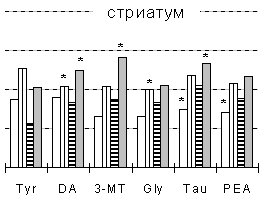
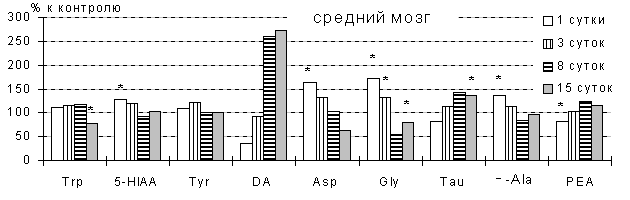
Рис. 3. Сдвиги содержания
биогенных аминов, их метаболитов, предшественников и свободных аминокислот
в в отделах головного мозга крыс в динамике ежедневного внутрибрюшинного
введения Tau в дозе 1/10 LD50.
Наряду с увеличением DA в стриатуме, содержание
Tau в стволе мозга (на 1 и 8 сутки) и в стриатуме (на 1, 8 и 15 сутки)
положительно коррелировало с содержанием DA и его метаболитов (DOPAC и
HVA), что говорит об активации в этих отделах мозга дофаминовой системы,
включающей усиление как синтеза (положительная корреляция Tyr - DA на 1
и 3 сут), так и распада медиатора; к концу эксперимента усиливается синаптический
выброс DA в стриатуме (повышение уровня 3-MT). В стволе мозга на 3 - 8
сут нарушалась корреляция 5-HT - 5-HIAA; последняя, а также связи Tau -
5-HT, Tau - 5HIAA, Trp - 5-HT появлялись к 15 сут. В стриатуме на 3 сут
нарушались корреляции 5HTP - 5-HT и Trp - 5HT.
В гипоталамусе на 1 и 3 сут нарушалась корреляционная
связь DOPAC - HVA, на 3 и 8 сут - связи Tau - 5-HT и Tau - 5HIAA, и на
3, 8 и 15 сут - Trp - 5-HT и 5-HT - 5-HIAA. Таким образом, изменение функционирования
серотониновой системы в гипоталамусе под действием Tau, вероятнее всего,
включает в себя угнетение синтеза медиатора и его деградации. Можно предполагать
также нарушение нормальных соотношений между показателями систем тормозных
и возбуждающих трансмиторов (исчезновение в гипоталамусе на сроках 1 -
8 суток корреляции Tau - GABA и на 8 сутки - Tau - Asp и Tau - Glu).

Рис. 4. Изменения содержания
биогенных аминов, их метаболитов, предшественников и свободных аминокислот
в отделах головного мозга крыс в динамике субконъюнктивального введения
Tau в суммарной дозе 1/10 LD50.
Ежедневное субконъюнктивальное введение Tau не
вызвало повышения его содержания в отделах мозга что, в определенной мере,
может объясняться появлением положительной корреляции между его уровнем
и уровнем его транспортного антагониста, Ala, зарегистрированной в стволе
мозга и стриатуме. На 3 сут во всех отделах мозга повысилось содержание
Trp, в гипоталамусе - GABA, в стриатуме и гипоталамусе - Ala (рис. 4).
Содержание возбуждающих трансмиттеров Asp и Glu увеличивалось на 1 сутки
опыта в стволе мозга и уменьшалось в стриатуме на 3 сутки, в сроках опыта
8 и 15 сут изменений в определяемых показателях не зарегистрировано. При
этом в стволе мозга на 1 и 3 сутки возникала положительная корреляция Tau
- Asp, одновременно в гипоталамусе нарушалась положительная корреляция
Tau - GABA, что свидетельствует об дисбалансе в содержании тормозных и
возбуждающих аминокислот-трансмиттеров. В стволе мозга возникала положительная
корреляция между уровнем Tau и уровнями DA и его метаболитов, что, возможно,
свидетельствует об активации в этом отделе мозга дофаминовой системы. Таким
образом, данные настоящего исследования свидетельствуют, что:
- дополнительное внутрибрюшинное введение таурина
в фармакологически активных дозах в течение 15 суток приводит к увеличению
в плазме крови концентрации незаменимых аминокислот - треонина и лизина,
концентрации аланина в плазме крови и печени, активирует синтез эндогенного
таурина в печени и практически не влияет на аминокислотный фонд сердечной
и скелетной мышц; активирует в печени и целом мозге реакции утилизации
углеродных скелетов аминокислот в цикле трикарбоновых кислот. Активация
дофаминовой системы в стриатуме и стволе мозга при данном способе введения
включает усиление как синтеза, так и распада медиатора, изменение функционирования
серотониновой системы в гипоталамусе включает торможение синтеза и деградации
медиатора.
- субконъюнктивальное введение таурина на протяжении
15 суток в суммарной дозе 1/10 LD50 вызывает дисбаланс в содержании
тормозных и возбуждающих аминокислот-трансмиттеров в среднем мозге, гипоталамусе
и стриатуме и кратковременное повышение содержания триптофана, практически
не оказывая влияния на процессы формирования аминокислотного фонда в периферических
тканях, что свидетельствует о возможности частичного воспроизведения нейрохимических
эффектов таурина при данном способе его введения.
ЛИТЕРАТУРА
-
Бенсон Дж. В., Патерсон Дж.А. Хроматографический
анализ аминокислот и пептидов на сферических смолах и его применение в
биологии и медицине. // Новые методы анализа аминокислот, пептидов и белков
/ Под ред. Ю.А. Овчинникова. - М., 1974.
-
Гуревич В.С. Таурин и функция возбудимых клеток.
- Л.: Наука, 1986.
-
Дорошенко Е.М. Формирование фонда биогенных аминов
и нейроактивных аминокислот в головном мозге крыс при алкогольной интоксикации
и отмене этанола. Автореф. дисс. … канд. биол. наук. Минск, 1994.
-
Методы биологии развития, под ред. Б.Л.Астаурова
и др. // М. Наука, 1974.
-
Мосолова И.М., Горская И.А., Шольц К.Ф., Котельникова
А.В. Получение прочно-сопряженных митохондрий из печени крыс, стабильных
при хранении. // Вопр. мед. химии. - 1971. - Т.17., №3.
-
Нефёдов Л.И. Формирование фонда свободных аминокислот
и их производных в условиях метаболического дисбаланса: Автореф. дисс...
д-ра медицинских наук. - Минск, 1993.
-
Островский Ю.М. Тиамин // Экспериментальная витаминология
/ под ред. Ю.М.Островского. - Минск, 1979.
-
Поздеев В.К. Медиаторные процессы и эпилепсия. -
Л.: Наука, 1983.
-
Раевский К.С., Георгиев В.П. Медиаторные аминокислоты
- М.: Медицина, 1986.
-
Справочник по клинической химии / Колб В.Г., Камышников
В.С. - Минск - Беларусь, 1982.
-
Таурин (фармакологические и противолучевые свойства)
/ Ярцев Е.И., Гольдберг Е.Д., Коменников Ю.А. - М.: Медицина, 1975.
-
Факторный, дискриминантный и кластерный анализ /
Ким Дж.-О., Мьюллер Ч.У., Клекка У.Р., Олдендерфер М.С., Блоэтфилд Р.К.:
Под ред. И.С. Енюкова. - М.: Финансы и статистика, 1989.
-
Azuma J., Sawamura A., Awata N. Usefulness of taurine
in chronic congestive heart failure and its prospective application //
J. Circ. J. - 1992. - V.56, N.1.
-
Azuoma I., Halliwell B., Haey B.M. The antioxidant action
of taurine, hypotaurine and their precursors // Biochem.J. - 1988. - V.256,
N.1.
-
Bergmeyer H.U. Methoden der enzymatischen Analyse. -
1962.
-
Cremer J.E., Jeal A.M. The activity of pyruvate dehydrogenase
in rat brain during postnatal development // FEBS Lett. - 1974.
-
Dorvil N.P., Yousef I.M., Tuchweber B. Taurine prevents
cholestasis induced by lithocholic acid sulfate in gunea pigs // Amer.
J. Clin. Nutr. - 1983.
-
Gentile S., Bologna E., Terracina D., Angelico M. Taurine-induced
diuresis and natriuresis in cirrhotic patients with ascites // Life Sci.
- 1994.
-
Glowinsky J., Iversen L.L. Regional studies of catecholamines
in the rat brain. The disposition of [H]-norepinephrine, [H]-dopamine and
[H]-DOPA in various regions of the brain // J.Neurochem. - 1966.
-
Hayes K.C., Sturman J.A. Taurine in metabolism // Ann.
Rev. Nutr. - 1981.
-
Huxtable R.J. Physiological action of taurine // Physiol.
Rev. - 1992.
-
Kozumbo W.J., Agarwal S., Koren H.S. Breakage and binding
of DNA by reaction products of hypochlorous acid with alanine, L-naphthylamine
or L-naphthol // Toxic. Appl. Pharmac. - 1992.
-
Nakashima T., Seto Y., Toshikazu N., Shima T., Iwai
Y., Zeizo K., Okanque T., Kashima K. Calcium-associated cytoprotective
effect of taurine on the calcium and oxygen paradoxes in isoleted rat hepatocytes
// Liver - 1990.
-
Naskalski J.W. Myeloperoxidase inactivation in the course
of catalysis of chlorination of taurine // Biochem. Biophys. Acta. - 1977.
- V.485.
-
Oja S.S., Korpi E.R. Amino acid transport // Hand. Neurochem.
- N.Y., 1983.
-
Reitmann S., Frankel S. A colorimetric method for the
determination of serum glutamic oxaloacetic and glutamic pyruvic transaminases
// Am. J. Clin. Path. - 1957.
-
Remme W.J. Congestive heart failure. Drug therapy: central
or peripheral approach? // Cardiolagia. - 1993. - V. 38, N.12, Suppl.1.
-
Sato Y., Ogata E., Fujita T. Hypotensive action of taurine
in DOCA-salt rats - involvement of sympathoadrenal inhibition and endogenous
opiate // Jpn. Circ. J. - 1991. - V.55, N.5.
-
Tenaglia A., Cody R. Evidence for taurine-defeciency
cardiomyopathy // Am. J. Cardiol. - 1988.
-
Thorne C.J.R., Dent N.J. Malate dehydrohenase isoenzymes
distribution in rat tissues. In: Enzymes and isoenzymes: Propeties, structure,
function / Ed. Shugar D. - A.P., L., N.Y., 1970.
-
Timbrell J.A., Seabra V., Waterfield C.J. The in vivo
and in vitro protective propeties of taurine // Gen. Pharmac. - 1995.
-
Wang W. Y., Liaw K.Y. Effect of a taurine-supplemented
diet on conjugeted bile acids in biliary surgical patients // J. Parenter.
Enteral. Nutr. - 1991.
-
Yamamoto S., Ohmoto K., Ideguchi S. Yamamoto R., Mitsui
Y., Shimabara M., Iguchi Y., Ohumi T., Takatori K. Painful muscle cramps
in liver cirrhosis and effects of oral taurine administration // Nippon
Shokakibyo Gakkai Zasshi. - 1994.
SUMMARY
V.Yu.Smirnov 1,
L.I.Nefyodov
1, Е.М.Doroshenko
1, I.I.Klimovich
2
POOL OF FREE AMINO
ACIDS AND THEIR DERIVATIVES UNDER CONDITIONS OF EXCESSIVE INTAKE OF TAURINE
1 Institute of Biochemistry National
Academy of Science of Belarus,
2 Grodno State Medical Institute
Key words: taurine, free amino
acids, biogenic amines, brain, liver, blood plasma, neurotransmitters.
The intraperitoneal Tau administration in
pharmacological active doses during 15 days leads to increase of nonessential
amino acids concentrations (Thr, Lys) in blood plasma, increase of concentrations
of Ala in the blood plasma and liver, activate an endogenous Tau syntheses
in liver and practically does not change heart and skeleton muscles amino
acid pool; activates glycolysis and utilization
of amino acids carbon chains in
tricarboxylic acid cycle in peripheral tissues and the whole brain.
It also activates dopamine system in
brain striatum and stem, changing a function of serotonin system in hypothalamus,
including inhibition of both syntheses and degradation of the mediator.
The 15 days subconjunctival
Tau administration
in total amount of 1/10 LD50 causes
an imbalance
in the contents of both inhibitory
and excitatory neurotransmitters in brain regions,
as well as short-term increase of Trp concentration,
however, practically not affecting
on processes of formation
of amino acids
fund in peripheral tissues, that might be evidence
of possibillity of partial reproducing of the neurochemical effects of
Tau under the given way of its administration.
This page hosted by 
Get your own Free Home Page





