КЛИМОВИЧ Иосиф Иосифович
СВОБОДНЫЕ
АМИНОКИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ В ПАТОГЕНЕЗЕ И ЛЕЧЕНИИ ОБЛИТЕРИРУЮЩЕГО АТЕРОСКЛЕРОЗА
СОСУДОВ НИЖНИХ КОНЕЧНОСТЕЙ
(клинико-экспериментальное исследование)
Гродненский
Государственный медицинский институт, кафедра факультетской хирургии
Институт
биохимии Национальной Академии наук Беларуси, лаборатория аналитической
биохимии *
Атеросклероз и возникающие на его почве сердечно-сосудистые заболевания за последние десятилетия стали одной из самых актуальных проблем медицины и здравоохранения во всех высокоразвитых странах мира [Богмат Л.Ф., 1997, Виноградов В.В., 1985, Ковшарь Ю.А., 1997, Либерман И.С., 1992, Репин В.С., 1989, Aston N.O., 1992]. Практически во всех странах наблюдается рост заболеваемости атеросклерозом [Кошкин В.М., 1991, 1994, Репин В.С., 1989, Чазов Е.И., 1995, Nobusto Y., 1997, Xavier P., 1997]. Только в США и странах СНГ в течение XX столетия от атеросклероза и его осложнений умерло более 350 млн. человек [Чазов Е.И., 1995].
Рост числа больных атеросклерозом и его осложнениями определяет и высокую смертность, причинами которой являются отсутствие стройной и доказанной теории патогенеза атеросклероза и концепции адекватной метаболической терапии и профилактики. В фундаментальных исследованиях не решены главные задачи: расшифровка действия основных факторов заболевания на уровне биорегуляторных систем, рецепторов и клеток; взаимоотношения между начальными биохимическими сдвигами в организме и морфологическими изменениями в сосудах; роль медиаторных процессов в регуляции гемостаза, тромбоза и репарации сосудов. Отсутствие ранних, адекватных и высокочувствительных методов диагностики не позволяет обосновать содержание целенаправленного корригирующего воздействия [Зозуля А.А., 1994, Зыков Д.В., 1992, Затевахин И.М., 1997, Чазов Е.И., 1995, Шанина Е.Ю., 1997, Carter S.A., 1996, Lassila R., 1989].
Имеются генетические линии лабораторных животных, подверженных атеросклерозу в злокачественной форме; несомненна роль наследственной предрасположенности и у человека, включая детерминированность локализации основных поражений [Анестиади В., 1982, Климов А.Н., 1995, Кошкин В.М., 1994, Кудрявцева И.В., 1995]. С другой стороны, у людей определенных расовых и этнических групп (коренные народы Севера) практически не наблюдалось атеросклероза, несмотря на традиционный для этих народов выосокоатерогенный рацион; в то же время у них в последние десятилетия заболеваемость атеросклерозом резко растет в связи с алкоголизацией [Чазов Е.И., 1991]. Имеются явные половые различия в преимущественной локализации атеросклеротических изменений: у женщин - сосуды головного мозга и сердца, у мужчин - ветви брюшной аорты, включая сосуды нижних конечностей [Прокубовский В.И., 1994, Чазов Е.И., 1991]. ОАСНК составляет около 50% от всей сердечно-сосудистой патологии [Виноградов В.В., 1985].
Одной из фундаментальных задач исследования патогенеза атеросклероза является поиск ранних биохимических критериев долипидной стадии атеросклероза, при которой морфологические изменения можно рассматривать как обратимые, а какие-либо клинические проявленя отсутствуют, и которая наблюдается в юношеском или молодом возрасте [Анестиади В., 1982, Богмат Л.Ф., 1997].
Лечение ОАСНК оставляет желать лучшего. Оперативное лечение помогает устранять только осложнения атеросклероза. Удельный вес таких больных невысок, основная масса больных лечится консервативно. Результаты консервативного лечения не могут считаться хорошими, поскольку количество больных, теряющих трудоспособность, и процент ампутаций конечностей не уменьшаются [Белов Ю.В., 1992, Бранд Я.Б., 1995, Гостищев В.К., 1993, Прохоров Г.Г., 1994, Ouriel K., 1994].
Интерес к изучению метаболических процессов, определяющих закономерности формирования фонда свободных аминокислот и их производных, обусловлен тем, что, во-первых, установлено, что первичным при атеросклерозе является нарушение не липидного, а белкового обмена [Репин В.С., 1989]; во-вторых, аминокислоты являются наиболее важными соединениями, участвующими в метаболизме азота и синтезе большинства эндогенных биорегуляторов: регуляторных белков, ферментов, гормонов, азотистых оснований, ряда нейромедиаторов и др. [Мусил Я., 1981, Bender D.A., 1975, Wurtman, 1980]. Экзогенно поступающие аминокислоты, окисляясь, участвуют в энергообеспечении организма и подвергаются многочисленным превращениям [Lubec C., 1990]. Обмен аминокислот довольно жёстко контролируется различными биохимическими и физиологическими механизмами, определяющими относительно постоянные их концентрации в крови (аминокислотный пул) и тканях (аминокислотный фонд) [Bender D.A., 1975, Holden J.T., 1962]. Изменениями в формировании аминокислотного пула сопровождаются практически все обменные нарушения. Стабильность фонда свободных аминокислот имеет весьма важное значение в реализации пластических функций клетки, особенно в биосинтезе белка и регуляторных пептидов. Сами аминокислоты и их дериваты часто выступают в роли аллостерических регуляторов, нейротрансмиттеров или их предшественников [Lubec C., 1990, De Feudis F.V., 1981, Perry T., 1982].
Пул свободных аминокислот физиологических жидкостей и аминокислотный фонд тканей млекопитающих является частью лабильной смешанной фазы низкомолекулярных интермедиатов обмена веществ и представлен набором метаболически и функционально взаимосвязанных соединений [Мусил Я., 1981, Isukada K., 1971]. В силу этого концентрации свободных аминокислот и их производных в физиологических жидкостях и тканях могут являться своеобразным интегральным показателем гомеостаза, а закономерности формирования аминокислотного фонда в организме - объективно отражать состояние метаболического баланса. Концентрация свободных аминокислот и их производных сама по себе является регулирующим фактором многих узловых пунктов метаболизма [Кричевская А.А., 1983].
Избыток аминокислот, поступающих с пищей, быстро удаляется из организма или катаболизируется в реакциях промежуточного обмена. Поэтому аминокислотам принадлежит связующая роль в интеграции основных метаболических потоков (гликолиз, глюконеогенез, липолиз, липогенез, цикл трикарбоновых кислот) [Кричевская А.А., 1983, Березов Т.Т., 1983, Нефёдов Л.И., 1991].
Сдвиги уровней отдельных аминокислот при атеросклерозе могут быть вызваны как алиментарными, так и метаболическими причинами. Наиболее разработанная в настоящее время липопротеидная теория атеросклероза практически не учитывает то, что в патогенезе окклюзионных заболеваний существенное значение имеют агрегация форменных элементов крови (прежде всего - тромбоцитов) и тромбирование артерий [Климов А.Н., 1995]. В механизмах указанных процессов ведущая роль принадлежит биологически активным соединениям эндогенного происхождения, в первую очередь - нейроактивным соединениям - аминокислотам и их производным - биогенным аминам. Их роль в регуляции сосудистого тонуса, активности реакций утилизации липидов, всасывания и утилизации холестерина не вызывает сомнений [Якунин Г.А., 1990, Чазов Е.И., 1991]. Тромбоциты отличаются избирательно высоким содержанием нейроактивных соединений (таких, например, как таурин, норадреналин, гистамин, серотонин) [Green J.P., 1989, Huxtable R., 1992, Franconi F., 1992]. Нарушения структуры эндотелия, морофологически определяемые в долипидной стадии атеросклероза, могут быть связаны и с нарушением функции тромбоцитов [Адамчик А.С., 1991, Анестиади В., 1982, Muller M.J., 1977].
Элементарные клеточные проявления атеросклероза удается воспроизвести in vitro с помощью фармакологических препаратов, действующих через активацию рецепторов или через систему передачи сигналов внутрь клетки [Atahanov S.E., 1992]. Реализация рецепторных взаимодействий осуществляется, как известно, на уровне клеточных мембран. Мембранотропные (стабилизирующие) свойства присущи в значительной степени многим биологически активным соединениям. В особенности это характерно для серусодержащих аминокислот и продукта их деградации - таурина [Нефёдов Л.И., 1992, Azuma J.,1988, Kurijama K., 1982].
Основное значение в регуляции метаболических потоков в настоящее время придается соотношению между уровнями указанных соединений в плазме крови и клетке, количеством их свободных и нековалентно связанных с различными клеточными структурами форм [Нефёдов Л.И., 1993, Airchart Y., 1974, Harper A.E., 1983]. Так, например, известно, что регуляторные свойства большинства нейроактивных соединений определяются не только отношением концентраций тормозные/возбуждающие, но и их свободными и связанным внутриклеточным пулом [De Feudis F.V., 1981, Perry T., 1982]. Исследование закономерностей этих явлений позволило бы не только выявить маркерные показатели начальных этапов атеросклероза, но и определить причино-следственные связи в последовательности реакций патогенеза этого заболевания.
В профилактике и лечении атеросклероза и его осложнений одно из ведущих мест отводится антиоксидантам природного происхождения [Репин В.С., 1989]. Известно, что к последним в первую очередь относятся серусодержащие аминокислоты и их дериваты [Lubec C., 1990, Blackburn G.L., 1983, Cooper A.J.L., 1983., Нефёдов Л.И., 1992]. В связи с этим актуальным является исследование механизмов реализации биологической активности и формирования внутриклеточного фонда важнейшего продукта деградации серусодержащих аминокислот - таурина [Lubec C., 1990, Нефёдов Л.И., 1990,1992, Гуревич В.С., 1986, Hayes K., 1981, Huxtable R., 1976]. Так, показано, что при введении таурина он оказывает гиполипидемическое и гипохолестеринемическое действие, активирует реакции всасывания и утилизации липидов и холестерина [Гуревич В.С., 1986, Ярцев Е.И., 1975, Azuma J., 1988]. Кроме того, нейромодуляторные свойства и высокие концентрации таурина в тромбоцитах определяют его участие в процессах агрегации, тромбирования артерий и регуляции сосудистого тонуса [Huxtable R., 1976].
Вышеперичесленное определяет актуальность исследования, обосновывает выбор предмета исследования, объектов (аминокислоты и их производные) и уровня (организменный, клеточный - тромбоциты) [Адамчик А.С., 1991, Якунин Г.А., 1990].
Целью работы было выяснение роли нарушений в формировании аминокислотного пула в патогенезе облитерирующего атеросклероза сосудов нижних конечностей и разработка методов целенаправленной коррекции аминокислотного фонда в комплексной метаболической терапии атеросклероза сосудов нижних конечностей.
Для реализации поставленной цели были определены следующие задачи:
Материалы и методы исследования
Экспериментальные модели. В опытах использовались крысы-самцы массой 140-200 г и кролики-шиншила, полученные из питомника АМН СССР "Рапполово" и содержавшиеся на стандартном рационе вивария со свободным доступом к воде.
Избыточное содержание Тау in vivo моделировали путем однократной внутрибрюшинной инъекции этого соединения в дозе, равной 1/10 LD50 (650 мг/кг) на 30 мин [Нефёдов Л.И., 1993].
Экспериментальная модель атеросклероза реализована на 30 белых крысах-самцах и 40 кроликах-шиншила при содержании животных на рационе, в состав которого входили 10% холестерина, 30% говяжего жира и 0,005% мерказолила [Горев Н.Н., 1972]. Таурин вводили внутрибрюшинно в дозе 650 мг/кг ежедневно, перорально в течение всего периода моделирования (60 сут) экспериментального атеросклероза. Контролями служили группы животных, получавшие изотонический раствор NaCl или обычный пищевой рацион.
Всего в экспериментах использовано 64 крысы и 40 кроликов.
Общая характеристика клинических исследований. Положения и выводы работы основаны на результатах обследования и лечения 411 больных, которые находились на лечении во II городской больнице, больнице скорой медицинской помощи, IV клинической больнице г.Гродно с 1990 по 1997 гг. Общая характеристика больных представлена в таблице 1.
Таблица 1
| Стадия |
|
|
|
|
Всего | |
| кол-во больных |
|
|
|
|
|
|
| Пол | м |
|
|
|
|
|
| ж |
|
|
|
|
|
|
| Возраст | 31-40 лет |
|
|
|
|
|
| 41-59 лет |
|
|
|
|
|
|
| 60 и более лет |
|
|
|
|
|
Критериями отбора больных, которым проводились предлагаемые методы лечения были: возраст до 80 лет, отсутствие сопутствующей соматической патологии внутренних органов в стадии декомпенсации, согласие больного на приём препарата [Дрюк Н.Ф., 1994]. Критерий исключения: индивидуальная непереносимость препарата. Продолжительность приема препаратов: 21 день. На фоне традиционного лечения больным назначалась питательная смесь "Тонус-1", обогащенная таурином (2 г/100 г смеси) по 15г 3 раза в день, или таблетки таурина (0,5 - по 1 таблетке 3 раза в день), или комбинированный аминокислотный препарат "Полиамин" (400,0 мл внутривенно капельно - 8-10 инфузий), или сочетание полиамина с таблетированным таурином.
В диагностике ОАСНК использовали данные общеклинического обследования, реовазографии (РВГ), УЗИ сосудов, ангиографии.
Контрольные группы были сформированы из 109 доноров станции переливания крови, от которых получена плазма.
Всего обследовано 520 человек.
Забор экспериментального материала для исследования. Крыс забивали декапитацией. Кровь (200 мкл) собирали в пробирки с 6% HClO4 для определения концентраций пирувата и лактата; затем собирали в гепаринизированные пробирки и получали плазму центрифугированием на холоду [Колб В.Г., 1982]. Образцы тканей (печени, скелетной мышцы, миокарда, отделов головного мозга) забирали в течение 1 мин после забоя и фиксировали в жидком азоте, часть печени и мозга (1-2 г) помещалась на лед для субклеточного фракционирования.
Оборудование и реактивы. В работе использовали: стандарты аминокислот, биогенных аминов и их метаболитов фирм Fluka, Serva, Sigma, Reanal; Calbiochem остальные реактивы - отечественного производства (квалификации не ниже хч) или фирмы "LaChema" (Чехия). 35S - цистеин) поставлен фирмой "Amercham", 14С- таурин - ВО "Изотоп". Аналитические колонки для ВЭЖХ фирмы "Элсико" (Россия). Кофермент А - фирмы "Fluka", НАД+ и НАДН - "Reanal". Органические растворители имели квалификацию "осч для жидкостной хроматографии". Экстракционные среды, подвижные фазы и растворы стандартов готовили с использованием воды для ВЭЖХ, полученной тройной дистилляцией в стеклянном аппарате с последующим пропусканием через патрон "Norganic" и фильтрованием через мембранный фильтр HATF 0,45 мкм (Millipore, США). Хроматографические определения проводили на хроматографе Waters (система подачи растворителя М501, модуль термостатирования колонок ТСМ, инжектор Rheodyne 7125, электрохимический детектор М460, Waters Assoc., США) и автоматическом анализаторе аминокислот Т-339 (Чехия). Прием и обработка хроматографических данных осуществлялась с помощью программно-аппаратного комплекса "МультиХром-1" (а/о "МультиХром", г.Москва; версия программного обеспечения - 2.67).
Анализ аминокислот в плазме крови и периферических тканях. Плазму депротеинизировали добавлением равного объема 1M НСlО4 (содержащей в качестве внутреннего стандарта норлейцин (n-Leu) 1250 нмоль/мл) и центрифугировали в течение 15 мин при 8000 об/мин. Нейтрализовали цитратным буфером (5 М, pH 3,0, 150 m л на 1мл образца). Образцы тканей гомогенизировали при 800 об/мин в гомогенизаторе со стеклянным пестиком в 10 объемах 0,2М HClO4, содержащей внутренний стандарт (n-Leu) из расчета 12,5 m М/г ткани. Безбелковые экстракты хранили при -20°С [Нефёдов Л.И., 1984, 1991].
Определение свободных аминокислот и их дериватов проводилась катионообменной хроматографией одноколоночным методом (колонка 22,0 х 0,35 см, сферический катионообменник LGAN 2B, 8 мкм ("Lachema", Чехия), элюирование последовательно осуществлялось Li-цитратными буферами. Скорость потока растворов 14 мл/час, температура дискретно повышалась в середине аналитического цикла с 40 до 62°С. Количественное содержание каждого компонента оценивалось по поглощению при длине волны 520 нм после реакции с 1% раствором нингидрина (скорость потока 12 мл/час) в капиллярной бане при 100°С [Нефёдов Л.И., 1991]. Калибровка системы осуществлялась по методу внутреннего стандарта с применением калибровочной смеси аминокислот фирмы "Calbiochem", США. Реагенты готовились из коммерческих комплектов для определения свободных аминокислот ("Lachema", ЧСФР) на деионизованной воде, которая перед использованием была подвергнута двойной дистилляции.
Определение биогенных аминов и их производных в плазме крови. Определение проводили в хлорнокислых экстрактах, содержащих ванилиновую кислоту (1 m М) и 3,4-диоксибензиламин (10 нМ) в качестве внутренних стандартов, методом ион-парной ВЭЖХ: колонка Сепарон SGX C18, 5 мкм, 3х150 мм с предколонкой 3х50 мм; подвижная фаза: 0,1 М KH2PO4, 17 мМ CH3COOH, pH 3,55, гептилсульфонат натрия 200 мг/л, октилсульфонат натрия 200 мг/л, ЭДТА 0,1 мМ, с добавлением 11,5 об.% метанола. Скорость потока 0,5 мл/мин, температура колонки 30°С. Детектирование электрохимическое, потенциал рабочего электрода 0,78 В, постоянная времени 1 с.
Метод ВЭЖХ биогенных аминов были разработаны к.б.н. Е.М.Дорошенко (1994).
Определение концентрации субстратов и активности ферментов. Митохондрии и гиалоплазму выделяли путем дифференциального центрифугирования при 10000 g из 10% гомогенатов в среде выделения (0,26 М сахароза - 0,01 М трис-буфер, рН 7,4, 0,001 М ЭДТА) [Островский Ю.М., 1978]. Определение активности аспартатаминотрансферазы и аланинаминотрансферазы проводили по методу Райтмана и Френкеля в модификации Колба В.Г.(1982). Активности ферментов ЦТК (MDH, IDH и GDH) определялась в печени и мозге в митохондриальной и гиалоплазматической фракциях спектрофотометрически по образованию или убыли восстановленных форм никотинамидных коферментов [Островский Ю.М.,1978].
Активность цистеинтрансаминазы в митохондриальной фракции определяли по количеству образующегося из пирувата аланина [Kurijama K., 1982], который определяли по короткой программе методом ионообменной хроматографии (элюция 0,3 М Li-цитратным буфером рН 2,95 при температуре анализа 62°С) в безбелковых экстрактах, полученных после центрифугирования при 3000 g. Активность цистеиноксидазы определяли в цитозольной фракции гомогенатов печени по количеству образующихся в процессе реакции цистеинсульфиновой и цистеиновой кислот, суммарное содержание которых определяли в безбелковых экстрактах методом ионообменной хроматографии (элюируются одним пиком 0,2 М Li-цитратным буфером рН 2,8 при температуре 39°С) [Нефёдов Л.И., 1993]. Активность цистеатдекарбоксилазы определяли в митохондриях радиометрическим методом по количеству поглощенного гиамином СО2.[Daniels, 1982] Радиоактивность определяли на жидкостно-сцинтилляционном счетчике Mark-2 (США).
Активности PDH и 2-OGD определяли в митохондриях печени феррицианидным методом [Островский Ю.М., 1978]. В отдельных случаях для сравнения активности ферментов определяли радиометрическим методом по количеству поглощенного гиамином СО2 в среде инкубации (0,2 мл I-14С-пирувата или 1-14С-a -кетоглутарата, МgCl2, НАД+, КоА, ТДФ, оксалоацетат, цитратсинтаза, рН 7,4).
Пируват определяли по методу, основанному на окислении NADH в присутствии избытка лактатдегидрогеназы (ЛДГ) [Островский Ю.М., 1984] по уменьшению экстинции при 340 нм.
Содержание глюкозы определяли энзиматически при сочетании гексокиназной реакции и окислении глюкозо-6-фосфата при помощи глюкозо-6-фосфатдегидрогеназы. Измерение количества восстановленного NADPH производилось спектрофотометрически при 340 нм. Гексозомонофосфаты определяли по методу Хохорста [Астауров Б.Л., 1974], основанному на сочетании глюкозо-6-фосфатдегидрогеназной и фосфогексоизомеразной реакций. В глюкозо-6-фосфатдегидрогеназной реакции по количеству восстановленного NADPH спектрофотометрически (при 340 нм) определялось содержание глюкозо-6-фосфата, после чего, с добавлением фосфогексоизомеразы в цепи двух реакций определялось содержание фруктозо-6-фосфата.
2-оксоглутарат (2-OG) определяли с помощью глутаматдегидрогеназы по убыли NADH в безбелковых экстрактах при l =340 нм. Митохондриальное соотношение свободных форм NAD+/NADH оценивали расчетным путем на основании глутаматдегидрогеназной реакции:
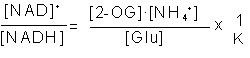
где К - константа равновесия для NAD+-зависимой глутаматдегидрогеназы [Великий Н.Н., 1987].
Уровень восстановленного глутатиона определяли по реакции сульфгидрильных групп с реактивом Элмана в кислотных экстрактах гомогенатов печени при 412 нм [Martensson J., 1985]. Общий фонд КоА определяли по реакции ацетилирования с ариламином [Островский Ю.М., 1978]. Ацетил-КоА и уровень свободной формы кофермента (КоАSH) определяли методом ВЭЖХ с градиентным элюированием и детектированием по поглощению при 254 нМ. Колонка Separon SGX C18 ("Элсико", СНГ) 5 мкм, 3 х 150 мм. Подвижная фаза: А - 50 мМ КН2РО4, В - ацетонитрил:вода 1:1 (об.). Скорость потока 0,5 мл/мин, температура - 30°С. Градиент 5-60% В, 12 мин [Дорошенко Е.М., 1991].
Содержание тиаминфосфатов определяли методом обращенно-фазной ВЭЖХ с постколоночной дериватизацией 0,3% К3[Fe(CN)6] в 15% NaOH с детектированием тиохромфосфатов по флуоресценции (360/450 нм). Использовали колонку Диасорб 130 С16Т, 3 х 150 мм, 8 мкм (Элсико). Состав подвижной фазы: 0,2 М КН2РО4, 40 мг/л ЭДТА, 400 мг/л гептилсульфоната натрия, 1,2% ацетонитрила.
Определение общих фосфолипидов и их фракций производили в липидном экстракте гомогенатов печени по содержанию липидного фосфора. Разделение фракций фосфолипидов производили в тонком слое силикагеля в системе хлороформ:метанол:вода (65:29:6). Антирадикальную активность оценивали по гашению вспышек быстрой люминесценции (в % ) при внесении возрастающих (10-6 - 10-2 М) концентраций тестируемого соединения в 0,14% спиртовой раствор олеата на хемолюминометре "ЛХМ 1Ц01". Таким же образом оценивали антиоксидантную активность гомогенатов печени по сравнению с контролем [Абакумов Г.З., 1990]. Концентрации холестерина и малонового диальдегида определяли по Колб В.Г и соавт.(1982).
Математическая
обработка результатов.
Для характеристики аминокислотного пула, кроме сравнения исследуемых
показателей с применением Т-критерия Стьюдента, использовали корреляционный
и линейно-дискриминантный анализ [Kim G.-O., 1989]. Внутригрупповые значения
корреляций считали достоверными при значениях |r| = 0,78 и выше. Значимость
отдельных показателей в выборке оценивали по значениям F-констант Фишера;
наличие различий между группами оценивали по матрицам классификации, а
также по расположению групп и отдельных реализаций в плоскости двух главных
компонент (по расстояниям D2 Махаланобиса). Перечисленные методы
были реализованы с помощью программ 3d и 7m из пакета ВМDР (BMDP Statistical
Software) [Dixon W., 1977].
Исследование фонда свободных
аминокислот и биогенных аминов при атеросклерозе в эксперименте и метаболические
эффекты таурина
Однократное введение Тау в фармакологически активной дозе (650 мг/кг) крысам вызвало увеличение его концентрации в печени и плазме крови в среднем в 2-3 раза. В плазме крови при этом увеличилось содержание цистеата, а уровни метионина, аланина, серина, АРУЦ и ААК снизились на 50%. В печени содержание цистеина не изменилось, а метионина и цистеата снизилось вдвое. В плазме и в печени уменьшилось количество серина и аланина, а треонина и глицина выросло; возникли высокодостоверные отрицательные связи (р<0,02, r = -0,85 - 0,90) в содержании гликогенных аминокислот и АРУЦ печени и плазмы крови. С позиций мембранотропных эффектов Тау возникшая метаболическая ситуация объясняется, прежде всего, активной экстракцией перечисленных аминокислот из кровеносного русла тканями, т.е. активацией в тканях метаболических процессов [Martensson J., 1985, Walser M., 1981]. В опытах in vitro Тау в концентрациях, соответствующих его уровню в тканях (10-4 - 10-6 М), проявлял выраженную антирадикальную активность, подавляя на 30-40% люминесценцию спиртового раствора олеата, вызванную Fe2+.. В гомогенатах печени опытных животных была достоверно выше суммарная антиокислительная активность; увеличилось содержание общих фосфолипидов и их фракций - фосфатидилхолина и сфингомиелина, уровень этаноламина снизился, а фосфоэтаноламина увеличился. Перечисленные изменения, так же как и продемонстрированное нами увеличение уровня восстановленного глутатиона и КоАSН, снижение соотношения в печени АРУЦ/ААК, конкурирующих за общие транспортные системы при их поступлении в клетку [Hayes, 1981], указывают на наличие мембранстабилизирующего, антиокислительного действия Тау.
Активность митохондриальных ЦТ и ЦД увеличивалась более чем в 1,5 раза, а активность конкурирующей за общий субстрат ЦО в цитозоле не изменилась, что, учитывая снижение метионина и цистеата в печени, позволяет сделать вывод о том, что Тау индуцирует процессы транссульфурирования [Ishimoto Y., 1979].
Активность митохондриальных ферментных систем, определяющих процессы окисления в ЦТК - глутаматдегидрогеназы, пируват- и 2-оксоглутаратдегидрогеназы на фоне введения Тау увеличивалась в 1,5-2 раза и в сумме с увеличением содержания 2-оксоглутарата и расчетной величины соотношения NAD+/NADH в митохондриях, уменьшением уровня глутамата, соотношения ацетил-КоА/КоАSН свидетельствует об активации процессов гликолиза и утилизации углеродных скелетов аминокислот в цикле трикарбоновых кислот [Hayes, 1981, Великий Н.Н., 1987]. Это подтверждается существованием в печени опытных животных положительных корреляционных взаимоотношений таурина с уровнем КоАSН, активностью пируватдегидрогеназы, соотношением NAD+/NADH и отрицательной - с уровнем тиаминдифосфата.
Таким образом, повышение концентрации Тау in vivo, вызванное его дополнительным экзогенным введением, активирует транспорт аминокислот из кровяного русла в ткани, процессы утилизации их углеродных радикалов в ЦТК и деградацию серусодержащих аминокислот, а также оказывает антиоксидантное действие, увеличивая содержание фосфолипидов и восстановленного глутатиона, что обосновывает применение Тау в качестве антиатерогенного средства.
Морфологическая картина изменений, возникших при моделировании атеросклероза, была следующей. При окраске суданом на поперечных и продольных срезах выявлены группы липидных гранул, по-видимому связанных с макрофагами. В венечных артериях встречаются незначительные локальные утолщения интимы. Реакция Окамото отрицательная. Наличие очагов липидных гранул в интиме аорты можно охарактеризовать как начальную стадию развития атеросклеротических изменений стенки кровеносного сосуда [Анестиади В., 1982]. В печени контрольной и опытной групп животных липидные включения определялись в группах гепатоцитов в перипортальной и частично в средней зонах печеночных долек. Таким образом, адекватность модельной ситуации экспериментального атеросклероза у крыс подтверждена патоморфологической характеристикой тканей, специфические изменения которых указывают на формирование атеросклероза. Кроме того, судя по значительному повышению уровней холестерина в печени и плазме крови, а также малонового диальдегида в печени и активностям основных метаболических реакций (гексокиназа, АСТ, АЛТ), концентрациям лактата и пирувата in vivo нами смоделирована адекватная атеросклерозу ситуация в обмене веществ [Климов А.Н., 1995, Цапенко М.В., 1994].
Введение таурина животным с экспериментальным атеросклерозом индуцировало патоморфологическую и биохимическую регрессию присущих данной патологии признаков. Содержание холестерина в печени и плазме крови и малонового диальдегида в печени снизилось до нормальных величин. Практически не отличалась от нормальных значений и активность гексокиназы, повышенная более чем в 2 раза в печени животных опытной группы. Таким образом, таурин обладает выраженными антиатерогенными свойствами при введении крысам в ситуации экспериментального атеросклероза. Это утверждение подтверждается результатами исследования пула свободных аминокислот в плазме крови и печени крыс. У опытных животных наболюдалось снижение содержания АРУЦ и повышение - тирозина, что указывает на снижение антитоксического индекса Фишера [Жадкевич М.М., 1989]. Также отмечался явный дефицит гликогенных аминокислот (серин, глицин) и снижение содержание глутамата. После введения таурина возвращалась к контрольным значениям концентрация серина, глицина, валина и лейцина, а также тирозина. Следовательно, таурин обладает способностью нормализовать величину антитоксического индекса Фишера, а также восстанавливать изменения в фонде гликогенных аминокислот, которые могут свидетельствовать о торможении глюконеогенеза при атеросклерозе [Шарманов Т.Ш., 1981].
В печени животных на фоне экспериментального атеросклероза было повышено содержание глутамата, аланина и снижено - глицина, этаноламина, фосфоэтаноламина и аммиака. Снижение содержания этаноламина может свидетельствовать либо о нарушении деградации серина, либо о снижении антиоксидантной защиты в печени [Авагимян Э.А., 1989, Быков И.Л., 1989]. Последнее является актуальным, учитывая однонаправлененость сдвигов в содержании АРУЦ (снижение их суммарного содержания) при неизменных концентрациях ароматических аминокислот. Повышение уровней глутамата и аланина может свидетельствовать об ингибировании глюконеогенеза в печени [Snell K., 1981].
Введение таурина приводило к повышению его содержания в печени, а также лейцина, изолейцина и цистина. Содержание фосфоэтаноламина нормализовалось. Таким образом, таурин обладал способностью уменьшать проявления метаболического дисбаланса в печени, включая увеличение содержания фосфоэтаноламина, а также нормализацию соотношения АРУЦ и ароматических аминокислот.
Нормализующее действие таурина на процессы формирования фонда свободных аминокислот и их производных в печени и плазме крови при атеросклерозе подтверждается данными линейно-дискриминантного анализа, где на основании значений D2-Махаланобиса очевидно, что назначение препарата значительно приближает исследованные показатели к контрольным значениям.
Исследование закономерностей формирования фонда нейроактивных соединений в отделах головного мозга показало, что введение таурина на фоне атеросклероза вызывало повышение содержания ГАМК в гипоталамусе при неизменном относительно атеросклероза содержании "возбуждающих" медиаторов (Asp и Glu), которые были достоверно повышены в среднем мозге животных. Это может свидетельствовать о нормализующем действии препарата на соотношение уровней "тормозных" и "возбуждающих" медиаторов в головном мозге при атеросклерозе, одним из звеньев патогенеза которого считают нарушения в ГАМК-ергической системе [Розанов В.А., 1988, Di Chiara G., 1981]. Кроме этого, при введении таурина наблюдался рост содержания триптофана, тенденция к повышению содержания 5-HT и 5-HIAA в среднем мозге и стриатуме, что свидетельствует об активирующем воздействии таурина на серотониновую систему, опосредованном повышением содержания предшественника [Wurtman R., 1980].
В среднем мозге введение таурина приводило к нормализации уровня тирозина, уровень которого был снижен при атеросклерозе. Так как известно, что повышением доступности тирозина удается активировать синтез катехоламинов в мозге [Chance W.T., 1990, Oishi T., 1984], можно предполагать модулирующее влияние таурина на эти показатели. Это подтверждается повышением содержания дофамина в стриатуме. После введения таурина отмечалось повышение содержания треонина в стриатуме и среднем мозге.
Практически важным выводом из данного этапа работы следует считать наличие у таурина адаптогенного действия на процессы формирования фонда свободных аминокислот и биогенных аминов при атеросклерозе. Тем самым, механизм действия препарата при атеросклерозе не исчерпывается его изветными эффектами.
Учитывая сложность моделирования развернутых проявлений атеросклеротических поражений сосудов у крыс, нами воспроизведена модель экспериментального атеросклероза у кроликов [Горев Н.Н., 1972], что позволило вызвать макроскопические изменения со стороны крупных артерий, вызывающие нарушения регионарного кровотока, следовательно, и те метаболические нарушения, которые являются следствием хронической гипоксии тканей, а не только самого атеросклероза как системной (обменной) патологии. Практически все клинические проявления атеросклероза и, в частности, ОАСНК, проявляются при появлении ишемических расстройств, которые возможны при наличии макроскопически определяемых поражений сосудов [Чазов Е.И., 1991].
При макроскопическом исследовании аорты животных опытной группы обнаружено: внутренняя поверхность аорты неровная за счет выступающих в просвет атеросклеротических бляшек и полосок с локализацией в области дуги, восходящем отделе аорты, в грудном отделе и брюшной части аорты в местах отхождений крупных кровеносных сосудов. Дефектов интимы и тромботических наложений не обнаружено.
Микроскопическая картина аорты в области локализации атеросклеротических бляшек у всех животных опытной группы имела однотипный характер: интима утолщена, особенно по краям липидной линзы. Липиды при окраске суданом черным В выявлялись в ксантомных клетках, а также экстрацеллюлярно. В области бляшек наблюдалась деструкция эластических волокон и разрастание соединительной ткани. Явлений атероматоза у экспериментальных животных не обнаружено.
Таким образом, в данном эксперименте удалось воспроизвести неосложненное атеросклеротическое поражение аорты с выраженной картиной липоидоза.
В плазме крови и тканях кроликов в ситуации экспериментального атеросклероза выявлен выраженный аминокислотный дисбаланс. В плазме крови животных опытной группы отмечалось достоверное снижение содержания таурина, а также цистина, серина, аспартата, глутамина, валина, лейцина и этаноламина. Это свидетельствует о дефиците серусодержащих аминокислот, не опосредованном снижением уровня предшественника [Stipanuk M., 1984]. Снижение соотношения АРУЦ и ароматических аминокислот, возможно, является признаком снижения антитоксической функции печени [Жадкевич М.М., 1989]. Таким образом, характер аминокислотного дисбаланса при экспериментальном атеросклерозе у кроликов не отличается от такового у крыс, у которых воспроизведены в основном метаболические нарушения, свойственные атеросклерозу. Однако, только у кроликов удалось выявить явный дефицит таурина. Так как содержание цистина было значительно снижено при нормальном уровне метионина, возможно, существует метаболический блок на уровне SAM-синтазы или реакций трансметилирования [Букин Ю.В., 1984].
В печени животных опытной группы также отчетливо выявлялся дефицит таурина, при этом содержание метионина и цистеиновой кислоты было выше контрольных значений, а цистина - снижено. Это, с одной стороны, подтверждает предположение об ингибировании синтеза цистеина [Wienstein C.L., 1988], а с другой стороны, позволяет предположить также торможение декарбоксилирования цистеата [Griffith O.W., 1983]. Таким образом, снижение синтеза таурина при экспериментальном атеросклерозе, очевидно, не обусловлено изменением соотношения между окислением и переаминированием цистеина [Ishimoto Y., 1979].
В ткани печени была снижена концентрация этаноламина, что не было обусловлено уровнем предшественника. Это позволяет предположить снижение антиоксидантных функций в печени (что дополнительно подтверждается низкой концентрацией цистина) [Быков И.Л., 1989]. Соотношение между концентрациями АРУЦ и ароматических аминокислот в печени изменялось однонаправленно с таковым в плазме крови за счет повышения уровня тирозина.
В сердечной мышце обнаружено существенное снижение содержания таурина (более чем в 3 раза) на фоне сниженного содержания как цистина, так и цистеата. Снижалось также содержание мочевины, глутамата, глутамина, гистидина и серина. Таким образом, дефицит таурина в сердечной мышце может быть обусловлен как снижением синтеза цистеина, так и перераспределением путей его превращений [Ishimoto Y., 1979]. Имеет место также выраженный дефицит гликогенных аминокислот.
Наконец, в скелетных мышцах кроликов имело место снижение содержания таурина на фоне неизменных концентраций цистина и цистеиновой кислоты и повышенной концентрации метионина. Повышалось содержание аммиака, тирозина и снижалось - серина.
Таким образом, в ситуации экспериментального атеросклероза у кроликов во всех исследованных тканях и плазме крови выявлен абсолютный дефицит таурина, механизмами развития которого могут быть торможение активности SAM-синтазы, перераспределение путей деградации цистеина в пользу его переаминирования, а также угнетение декарбоксилирования цистеата. Любой из этих механизмов, как и их сочетание, позволяет считать назначение метионина в данной ситуации метаболически необоснованным, так как основным нарушением в обмене серусодержащих аминокислот является дефицит таурина, который в данной метаболической ситуации не будет эффективно устраняться применением метионина. Кроме этого, более или менее постоянно наблюдалось снижение содержания в тканях глутамина, а также серина и/или этаноламина.
После применения таурина у кроликов с экспериментальным атеросклерозом макроскопические изменения стенки исследованных сосудов были менее выражены, чем при моделировании атеросклероза. Ни у одного животного после применения таурина при макроскопическом исследовании не были обнаружены бляшки в брюшном отделе аорты. Если у животных без применения таурина атеросклеротические бляшки практически сливались в восходящей части аорты, а также в начальном отделе грудной аорты, то у животных, получавших таурин, степень выраженности атеросклероза была значительно меньше. У этих животных наблюдались отдельные бляшки в области дуги и восходящем отделе аорты, а также в грудной части аорты.
Микроскопическая картина аорты в области локализации атеросклеротических бляшек была сходной у животных, получавших и не получавших таурин. Таким образом, морфологическая картина поражений сосудов у экспериментальных животных различалась по распространенности процесса [Petty M.A., 1990].
Применение таурина при экспериментальном атеросклерозе у кроликов приводило к повышению его содержания в плазме крови до контрольных значений. Нормализовалось также содержание цистина, а уровень цистеата стал ниже контрольных значений. Вернулись к контрольным значениям концентрации аспартата, валина и лейцина. Содержание треонина, серина, глицина и глутамина, а также изолейцина, повысилось выше контрольных цифр. Таким образом, таурин устранял сдвиг соотношения между концентрациями АРУЦ и ароматических аминокислот за счет повышения содержания АРУЦ. Устранялся также дефицит гликогенных аминокислот.
В печени кроликов после применения таурина на фоне атеросклероза его концентрация также нормализовалась, в то время как уровень цистеата имел тенденцию к дополнительному повышению. Содержание цистина оставалось сниженным. Это подтверждает наше предположение о том, что в печени одним из механизмов развития недостаточности таурина является торможение декарбоксилирования цистеата. Таким образом, назначение таурина представляется единственным возможным способом устранения дисбаланса уровней серусодержащих аминокислот в печени на фоне атеросклероза.
В сердечной мышце концентрации таурина, цистина и цистеата после его применения нормализовались. По сравнению с группой животных, не получавших таурин, повышалось содержание глицина, метионина и лейцина, а также нормализовались измененные при атеросклерозе уровни серина, аланина, глутамата, глутамина и гистидина. Таким образом, таурин при экспериментальном атеросклерозе обладал выраженным кардиопротекторным действием [Цезарь А.Е., 1995], устраняя практически все проявления аминокислотного дисбаланса при атеросклерозе. Основными его эффектами в данном случае является нормализация пула серусодержащих и повышение суммарного содержания гликогенных аминокислот.
В скелетных мышцах кроликов при применении таурина на фоне атеросклероза также происходила нормализация его уровня; содержание серусодержащих аминокислот-предшественников не изменялось, концентрация метионина оставалась повышенной. Повышалось содержание валина, нормализовалось - серина; снижалось - цистатионина, глутамата и фосфоэтаноламина. Снижение содержания цистатионина, обнаруженное нами в мышцах и сердце, может быть одним из механизмов нормализующего действия таурина на уровни серина и цистина - соединений, являющихся предшественниками цистатионина [Kurijama K., 1982].
Таким образом, применение таурина
в экспериментальной модели атеросклероза у кроликов оказалось весьма эффективным
с позиций его нормализующего действия на пул серусодержащих аминокислот,
гликогенных аминокислот и восстановление нормального соотношения АРУЦ и
ароматических аминокислот в печени и плазме крови. Применение таурина представляется
с метаболических позиций наиболее рациональным для ликвидации существующего
при атеросклерозе метаболического дисбаланса.
Клинико-лабораторные показатели
и формирование фонда свободных аминокислот и биогенных аминов больных ОАСНК
при традиционном лечении
Оценка общеклинических параметров у обследованных больных позволила выявить, что раннее развитие ОАСНК наблюдается практически исключительно у мужчин. С возрастом увеличивается количество больных, страдающих сопутствующими заболеваниями, особенно сахарным диабетом, ИБС и гипертонической болезнью. Все больные в возрасте менее 40 лет имели вредные привычки; их распространенность у больных более старших групп уменьшалась. Таким образом, для более молодых больных характерна высокая этиологическая роль вредных привычек (курения) [Lassila R., 1989], в то время как у пожилых больных возрастает роль сопутствующих заболеваний и заболевание сопровождается более тяжелыми проявлениями [Ковшарь Ю.А., 1997].
Данные общелабораторных исследований свидетельствуют, что у больных старше 60 лет концентрация фибриногена В при поступлении и при выписке была достоверно выше, чем в группе 41-59 лет, что может свидетельствовать о склонности к гиперкоагуляции. У больных старшего возраста при поступлении был выше тонус регионарных артерий мелкого калибра, что может свидетельствовать о развитии ишемического синдрома и недостаточном развитии коллатерального кровообращения. Более высокое содержание b -липопротеидов у больных старше 60 лет может свидетельствовать о более глубоком нарушении липидного обмена, причем оно регистрировалось и при выписке больных [Климов А.Н., 1995].
Время свертывания крови достоверно не изменялось ни в зависимости от длительности заболевания, ни в процессе лечения. Таким образом, состояние системы гемостаза, оцениваемое по обычным клиническим тестам, не претерпевает у исследованных болных существенных изменений и не зависит от давности заболевания.
Показатели стандартных клинических биохимических тестов практически не показывали отклонений от нормальных значений, не менялись в зависимости от давности заболевания.
Несмотря на то, что время свертывания крови и время рекальцификации не зависели от наличия и выраженности болей, содержание фибриногена А и, в большей степени, фибриногена В, было более высоким у больных с выраженным болевым синдромом. Такая тенденция сохранялась и к моменту выписки. Это свидетельствует о тромбоопасности у таких больных [Зыков Д.В., 1992] и диктует необходимость купирования болевого синдрома с целью профилактики тромбозов и ДВС-синдрома.
Все случаи гангрены наблюдались нами только у больных, которые могут пройти менее 100 м, что подтверждает высокую прогностическую значимость дистанции безболевой ходьбы [Бураковский В.И., 1989]. У больных, способных пройти менее 500 м, отмечался более высокий протромбиновый индекс, а к моменту выписки регистрировался более высокий уровень b -липопротеидов, т.е.традиционная терапия не устраняет одного из наиболее существенных нарушений липидного обмена у больных с большей выраженностью функциональных расстройств периферического кровообращения.
Парестезии и слабость в ногах чаще регистрировались у больных с недостаточностью кровообращения; наблюдалась четкая обратная зависимость длительности ремиссии от стадии недостаточности кровообращения. Прямая зависимость имела место для похолодания кожных покровов, цианоза, отсутствия пульсации на периферических сосудах, наличия шумов, трофических расстройств и гангрены. При недостаточности кровообращения III ст. повышался уровень фибриногена В. Реографический индекс при поступлении был существенно снижен при наличии недостаточного кровообращения; степень снижения зависела от стадии недостаточности. Аналогичная связь наблюдалась и для тонуса как магистральных, так и регионарных артерий. Это указывает на наличие тесной связи между клинически выраженной недостаточностью кровообращения и показателями, характеризующими степень функциональной недостаточности кровообращения в нижних конечностях.
Особый интерес представляет сравнение разультатов лабораторного и биохимического обследования больных в зависимости от стадии атеросклеротического поражения сосудов. Содержание тромбоцитов и время свертывания крови не зависели от стадии заболевания. Поскольку время свертывания крови не зависело ни от одного из проанализированных нами факторов, следует считать этот показатель неинформативным с точки зрения его диагностического и прогностического значения у больных ОАСНК. У больных II-IV ст. часто обнаруживался фибриноген В, причем частота его обнаружения практически не изменялась в процессе лечения. Реографический систоличекский индекс при поступлении имел четкую связь со стадией заболевания. К моменту выписки достоверные различия между стадиями исчезали, т.е. реографический индекс имел тенденцию к повышению. Повышенный тонус магистральных и регионарных артерий регистрировался в значительной части случаев при II - IV ст., причем тонус регионарных артерий был повышен практически равномерно как за счет сосудов крупного, так и среднего и мелкого калибра. Нами не было обнаружено различий в уровне b -липопротеидов и холестерина больных с различными стадиями атеросклероза. Очевидно, морфологические изменения сосудов, определяющие стадию заболевания, зависят не только или не главным образом от выраженности нарушений липидного обмена. Активности трансаминаз, содержание общего белка, сахара и билирубина не отклонялись от нормы и не изменялись достоверно в зависимости от стадии заболевания.
Таким образом, между определенными симптомами заболевания и степенью тяжести, отражающей морфологические изменения в сосудах, имеется достаточно тесная, но не абсолютная зависимость. Сахарный диабет, ожирение (независимо от степени) утяжеляют течение ОАСНК.
Содержание биогенных аминов, метаболитов дофамина, а также триптофана при поступлении больных не зависело от возраста, однако у больных старше 60 лет содержание норадреналина было ниже, чем адреналина. У больных со II стадией недостаточности кровообращения отмечалось низкое содержание норадреналина и адреналина при сравнительно высоком уровне дофамина. Можно предполагать, что развитие недостаточности кровообращения у больных атеросклерозом сопровождается угнетением гидроксилирования дофамина [Попович М.И., 1990]. Вероятно, регуляция сосудистого тонуса в этом случае осуществляется в большей степени за счет уровня дофамина, в то время как извесно, что ответ на введение адреналина таким больным может быть парадоксальным как на системном уровне, так и на уровне пораженного сосуда [Чазов Е.И., 1995]. Уровень дофамина при более выраженном болевом синдроме имел тенденцию к повышению. При дистанции безболевой ходьбы менее 100 м наблюдалось снижение содержания серотонина в плазме. Этот эффект еще более показателен, учитывая повышение этого показателя при выраженной недостаточности кровообращения, которая часто наблюдается у таких больных. Очевидно, метаболические расстройства, сопровождающие клинически выраженный атеросклероз, включают в себя уменьшение синтеза серотонина энтерохромаффинной тканью или усиление диоксигеназного расщепления триптофана в печени, вследствие которого происходит нарушение нормального соотношения двух основных путей превращения триптофана в сторону кинуренинового пути. Продукты последнего, возможно, способствуют увеличению болевой чувствительности или снижению переносимости физической нагрузки [Chaouloff P., 1986].
Уже при I стадии заболевания имеется выраженная тенденция к снижению содержания триптофана. Только при I стадии отмечалось снижение содержания серотонина. Отсутствие этого снижения у больных II-IV стадий можно предположительно связать с выходом дополнительных количеств серотонина в плазму из тромбоцитов, где его содержание, как известно, очень высокое. Содержание дофамина, а также 3,4-диоксифенилуксусной кислоты, было повышенным. Это может свидетельствовать о нарушении b -гидроксилирования дофамина и превалировании его окислительного дезаминирования [Ahtee L., 1985]. При всех стадиях заболевания было снижено содержание конечного метаболита дофамина - гомованилиновой кислоты. Таким образом, ряд сдвигов в содержании биогенных аминов, их предшественников и метаболитов в плазме крови имеется уже у больных I стадии. Очевидно структура и функции тромбоцитов в I стадии не нарушается, а в последующих II-IV происходит их нарушение.
При поступлении больных в плазме крови нами не было обнаружено достоверных различий в концентрации свободных аминокислот и их производных в зависимости от возраста больных, наличия и степени ожирения, недостаточности кровообращения. Однако, наличие недостаточности регионарного кровотока оказывает влияние на формирование аминокислотного фонда. Так, у больных с наиболее выраженным болевым синдромом отмечалось более высокое содержание мочевины, ароматических аминокислот, лизина и лейцина. В целом наблюдавшаяся тенденция к обогащению аминокислотного пула может объясняться наличием катаболической реакции, связанной с выраженной гипоксией тканей и распадом мышечного белка [Rivera S., 1988]. Таким образом, хроническая гипоксия тканей приводит к развитию аминокислотного дисбаланса. Однако, нами не было обнаружено зависимости от функциональных резервов компенсации, оцениваемых по дистанции возможной безболевой ходьбы. Очевидно, сдвиги в формировании аминокислотного фонда отражают не адаптационные резервы кровообращения, а степень выраженности гипоксии тканей.
У больных с давностью заболевания более 5 лет наблюдалась тенденция к снижению уровня таурина и достоверное снижение его основного предшественника - цистеиновой кислоты. Кроме этого, при большей длительности заболевания отмечалось общее обеднение аминокислотного пула в основном за счет аминокислот с разветвленной углеводородной цепью, ароматических аминокислот, а также глицина, орнитина и гистидина. Таким образом, вне зависимости от степени функциональной компенсации, сама по себе давность заболевания сопровождается развитием выраженного аминокислотного дисбаланса, причем его характер противоположен таковому, наблюдающемуся при выраженном болевом синдроме.
При I стадии заболевания зарегистрировано повышение уровня цистеата на фоне нормального содержания таурина, снижение содержания серина, аспарагина и глутамина (хотя концентрация глутамата была выше контрольных цифр). Содержание пролина было повышено, этаноламина и аммика, а также гистидина - снижено. Снижение содержания этаноламина можно объяснить снижением содержания его предшественника - серина [Мусил Я., 1981]. В этой стадии еще не наблюдалось определенного преобладания дефицита гликогенных аминокислот. Однако, можно предполагать функциональный дефицит таурина, исходя из повышения содержания его предшественника.
Во II стадии снижение аспарагина и глутамина сохранялось, причем концентрация последнего была достоверно ниже, чем при I стадии, а также повышалась концентрация цистатионина. Остальные сдвиги сохраняли ту же направленность, что и в I стадии.
После курса традиционного лечения у больных ОАСНК II ст. снижались концентрации метионина, цистина, цистеата и таурина по сравнению с их значениями при поступлении; кроме этого, снижались как по отношению к моменту при поступлегнии, так и к контролю, концентрации лейцина, изолейцина, глицина, орнитина и гистидина. Таким образом, имеющийся аминокислотный дисбаланс к концу курса традиционной терапии не только не устраняется, но и усугубляется: приобретает абсолютный характер дефицит серусодержащих аминокислот [Huxtable К., 1978], снижается содержание аминокислот с разветвленной углеводородной цепью. Ни одно из проявлений аминокислотного дисбаланса к концу лечения не имело тенденции к нормализации.
В III стадии направленность метаболических сдвигов сохранялась, однако, отмечался выраженный подъем концентрации цистеата. Это подтверждает наличие функционального дефицита таурина. Сохранялось также повышение концентрации цистатионина. После курса традиционного лечения, как и при II стадии, все сдвиги в концентрациях аминокислот сохранялись. Содержание цистеата и таурина достоверно снижалась по сравнению с моментом при поступлении. По сравнению с началом лечения уменьшалось содержание серина и увеличивалось - глутамата, что может быть расценено как усугубление проявлений аминокислотного дисбаланса.
Наконец, при IV ст. наблюдалось выраженное общее обеднение пула за счет преимущественно гликогенных аминокислот. Концентрация цистеата не отличалась от контрольных значений, а таурина - снижалась более чем в 3 раза. Это свидетельствует о том, что функциональная (относительная) недостаточность таурина становится абсолютной и обусловленной дефицитом предшественника [Huxtable R., 1978, Jacobsen J.C., 1968]. Существенно сниженными оказались также концентрации цистина и метионина, что подтверждает этот вывод.
Обращает на себя внимание, что при IV стадии снижалась концентрация не только аммиака, но и мочевины, хотя по отношению к концентрации остальных определяемых соединений концентрация аммиака увеличивалась. Исходя из этого факта, можно утверждать о превалировании катаболизма белка и свободных аминокислот, несмотря на сниженную (в абсолютных значениях) концентрацию аммиака [Дубикайтис А.Ю., 1993]. Все сдвиги в концентрациях исследованных соединений, имевшие место при поступлении этих больных по отношению к контролю, к моменту выписки сохранялись.
Таким образом, ОАСНК характеризуется выраженным аминокислотным дисбалансом в плазме крови, проявляюшимся обеднением пула в основном за счёт гликогенных и серусодержащих аминокислот, выраженность которого зависит от стадии заболевания. К моменту выписки аминокислотный дисбаланс у больных II-IV стадий не имел тенденции к ликвидации, а в ряде случаев его проявления становились более выраженными.
Известно, что при сахарном диабете многочисленные морфофункциональные изменения сосудистого русла при окклюзионных поражениях артерий усугубляются дефицитом инсулина и сопряжёнными метаболическими сдвигами [Розен В.Б., 1984]. Нарушения промежуточного обмена аминокислот и их производных при сахарном диабете исследованы относительно детально [Ньсхолм Э., 1977], а отдельные аминокислоты или их искусственные смеси уже рекомендуются для коррекции метаболического дисбаланса при этой патологии [Вретлинд А., Суджян А., 1990].
Больные ОАСНК II стадии с сопутствующим сахарным диабетом отличались значительно более выраженным аминокислотным дисбалансом, чем вся группа больных ОАСНК II стадии. У больных с сопутствующим сахарным диабетом наблюдалось снижение уровня таурина, хотя содержание цистеиновой кислоты было на уровне контрольных значений и достоверно ниже, чем у всех больных II стадии; снижение уровней мочевины, аспартата, аспарагина и цистина (достоверны по отношению как к контролю, так и ко всем больным ОАСНК II стадии); метионина, глицина, валина, изолейцина, лейцина и фенилаланина (достоверны по отношению к контролю, у всех больных II стадии эти изменения отсутствовали). Остальные изменения, наблюдавшиеся у обследованных больных ОАСНК II стадии, присутствовали и у больных с сопутствующим сахарным диабетом. Таким образом, сахарный диабет усугубляет проявления метаболического дисбаланса при ОАСНК, причем характер дисбаланса в целом был сходным и заключался прежде всего в дефиците серусодержащих и гликогенных аминокислот. Однако, дисбаланс уровней серусодержащих аминокислот уже при II стадии заболевания принимал характер, наблюдавшийся при IV стадии (абсолютный дефицит таурина). Кроме этого, при сахарном диабете наблюдалось снижение уровней АРУЦ.
Язвенная болезнь желудка и 12-перстной кишки способна сама по себе вызывать аминокислотный дисбаланс вследствие нарушения гормональной регуляции процессов всасывания и транспорта аминокислот [Лызиков А.Н., 1987]. Вследствие этого, мы выделили группу больных ОАСНК II стадии, страдающих сопутствующией язвенной болезнью желудка и 12-перстной кишки. Выявлено, что у этих больных имеются в основном однонаправленные сдвиги в уровнях исследованных соединений с таковыми у всей группы больных ОАСНК II стадии, однако, ряд изменений выражен в большей степени. Так, уровни серина, АРУЦ и ароматических аминокислот были достоверно снижены по отношению к контрольным значениям, хотя у всей группы больных ОАСНК II стадии таких сдвигов не было. Уровень цистеата, повышенный при II стадии ОАСНК, при наличии язвенной болезни был достоверно ниже и не отличался от контроля. Это позволяет предположить большую степень выраженности дисбаланса серусодержащих аминокислот у этих больных. Последнее подтверждается также значительным снижением содержания цистина, достоверным по отношению как к контролю, так и к больным ОАСНК II стадии. Аналогичные обнаруженным для цистеата сдвиги были обнаружены для концентрации аспартата; кроме этого, у больных с язвенной болезнью не отмечалось повышения концентрации глутаминовой кислоты. Это согласуется с литературными данными о снижении ее уровня у больных язвенной болезнью [Терехов Н.Т., 1984] и о ее эффективности для лечения язвенной болезни.
Вышесказанное означает, что при коррекции аминокислотного дисбаланса у больных ОАСНК II стадии с сопутствующей язвенной болезнью необходимо учитывать наличие существенного снижения содержания незаменимых аминокислот, а также функционального дефицита таурина.
В плазме крови больных ОАСНК, перенесших
ранее резекцию желудка, по сравнению со всей группой больных ОАСНК II стадии,
наблюдался выраженный дефицит серусодержащих аминокислот, причем были снижены
одновременно концентрации как таурина, так и цистеиновой кислоты. Был снижен
уровень аспартата, повышенный у всей группы больных ОАСНК II стадии, весьма
существенно снижен уровень цистина. В целом сдвиги в содержании исследованных
соединений были однонаправленными с таковыми, описанными выше для больных
с сопутствующей язвенной болезнью. Однако, после резекции желудка наблюдалось
более существенное снижение содержания этаноламина, достоверное по отношению
к контролю снижение уровня аспартата. Это позволяет говорить о том, что
после резекции желудка проявления метаболического дисбаланса, имеющегося
у больных ОАСНК при сопутствующей язвенной болезни, не устраняются. Из
этого следует важность их коррекции у больных, перенесших резекцию желудка,
аминокислотными препаратами, включая их в схему лечения ОАСНК.
Клинико-лабораторная характеристика
обследованных больных, формирование аминокислотного пула и метаболические
процессы при предлагаемых методах лечения облитерирующего атеросклероза
нижних конечностей
При выписке больных, получавших аминокислотные препараты (полиамин, таурин или их сочетание), весьма редко определялся фибриноген В (достоверно реже, чем при традиционной терапии). Протромбиновый индекс у больных, получавших традиционное лечение, находился на верхней границе нормы, в то время как у больных, получавших аминокислотные препараты или антиоксиданты, он был достоверно ниже. Это свидетельствует о том, что при применении аминокислотных препаратов нами достигалась практически полная ликвидация тромбоопасности, т.е. один из критериев ремиссии [Зыков Д.В., 1992], в то время как у больных контрольной группы такая компенсация достигалась далеко не всегда. Кроме этого, содержание b -липопротеидов у больных после применения аминокислотных препаратов было достоверно ниже, чем после традиционной терапии.
Сравнение различных способов лечения (традиционное, традиционное с применением антиоксидантов, с применением аминокислотных препаратов) показало, что при выписке после применения аминокислотных препаратов отмечалось повышение содержания серусодержащих аминокислот, обладающих свойствами эндогенных антиоксидантов (цистин, таурин), уменьшалась концентрация глутаминовой кислоты и увеличивалась - глутамина. Имели тенденцию к нормализации концентрации аланина и серина, повышалось содержание АРУЦ, гистидина и этаноламина. Выделенная нами подгруппа больных, получавших традиционную терапию с применением антиоксидантов, практически не имела статистически достоверных отличий от всей группы больных, которым не назначались аминокислотные препараты. Имелась даже тенденция к снижению в этой подгруппе содержания этаноламина и таурина - соединений, обладающих свойствами эндогенных антитоксидантов [Маньковская И.М., 1992, Ярцев Е.И., 1975].
Обнаруженное нами снижение содержания этаноламина во всех клинических группах, где оно регистрировалось, сопровождалось снижением концентрации серина. Тенденция к восстановлению уровня этаноламина, наблюдавшаяся нами после применения аминокислотных препаратов, также сочеталась со статистически достоверным повышением содержания серина. Это позволяет считать, что повышение уровня этаноламина, наблюдавшееся после применения полиамина и таурина, не является следствием деградации клеточных мембран [Ганиев Х.Г., 1986], а имеет метаболическое происхождение и может быть одним из эффектов нормализации фонда гликогенных аминокислот.
Исследования пула свободных аминокислот в плазме крови ___ больных ОАСНК, ___ из которых на протяжении месяца наряду с обычным лечением получали таурин, показали, что при его применении имеет место активация процессов детоксикации аммиака, мочевинообразования и цепи окислительно-восстановительных превращений серусодержащих аминокислот-гепатопротекторов. Кроме того, отчётливо заметна тенденция нормализации антитоксического индекса Фишера, а также восстановление высокодостоверных коррелятивных связей между концетрациями АРУЦ, которое в определённой степени свидетельствует о нормализации процессов детоксикации, протеолиза и реакций глюконеогенеза в печени и мышцах [Watanabe A., 1986].
При применении полиамина у больных ОАСНК II ст. к концу лечения наблюдалось повышение содержания триптофана, а также серотонина. Очевидно, оба эффекта метаболически взаимосвязаны; кроме этого, вероятна нормализация функции тромбоцитов как депо серотонина. К концу лечения повышалось соотношение концентраций норадреналина и адреналина за счет увеличения содержания норадреналина. Снижалось содержание 3,4-диоксифенилуксусной кислоты и повышалось - гомованилиновой кислоты, что свидетельствует об активации О-метилирования катехоламинов [Weiner N., 1989]. При применении таурина также отмечалось повышение содержания серотонина в процессе лечения, однако оно не было связано с изменением концентрации предшественника, а, очевидно, только с эффектами таурина на структуру и функцию тромбоцитов. Направленность сдвигов уровней катехоламинов была такой же, как и после введения полиамина, однако не повышалось содержание 3,4-диоксифенилуксусной кислоты.
Таким образом, введение как таурина, так и полиамина оказывает выраженный нормализующий эффект на содержание в плазме крови больных ОАСНК II ст. биогенных аминов, триптофана и кислых метаболитов дофамина. Одним из возможных механизмов такого восстановления может быть действие таурина на функции тромбоцитов [Ешкеева А.И., 1995].
Применение полиамина вызывало нормалмзацию концентрации глутамина, которая при поступлении была значительно ниже контрольных значений. Уровни треонина, валина, метионина, глицина и аспарагина также при поступлении были ниже контрольных значений и нормализовались к концу лечения. Концентрации серина, аланина, глутамина, этаноламина и гистидина хотя и достоверно повышались к концу лечения, оставались, тем не менее, ниже контрольных значений. Полиамин не оказал влияния на уровни серусодержащих аминокислот, кроме метионина.
Таким образом, значительная часть проявлений аминокислотного дисбаланса при ОАСНК II ст. после применения полиамина устраняется или имеет явную тенденцию к уменьшению. Однако, препарат не полностью устранял ряд наиболее существенных проявлений аминокислотного дисбаланса: дефицит гликогенных и серусодержащих аминокислот, а также соединений, обладающих свойствами эндогенных антиоксидантов. Примененный режим введения и дозы препарата оказались недостаточными для нормализации концентрации серина и этаноламина. Полиамин полностью нормализовал концентрацию метионина, однако был неэффективен для восстановления сниженной концентрации таурина. Учитывая тот факт, что концентрация таурина была сниженной на фоне более высокой, чем в контроле, концентрации цистеиновой кислоты, назначение самого таурина для коррекции его функционального дефицита представляется оправданным. Кроме этого, для целенаправленной метаболической коррекции нарушений, возникающих при атеросклерозе, рационально обогащение применяемых аминокислотных смесей гликогенными аминокислотами - серином и аланином.
Применение таурина на фоне традиционной терапии ОАСНК уже в середине лечения приводило его концентрацию к контрольным значениям. Содержание цистеиновой кислоты оставалось повышенным. Наблюдалось достоверное повышение уровня аспартата до контрольных значений уже к середине лечения. Однако, влияние таурина на уровень аспарагина и глутамина, хотя и было однонаправленным с таковым у полиамина, оказалось менее выраженным. Влияние таурина на концентрации серина, глицина, аланина и валина было аналогичным влиянию полиамина, что может свидетельствовать о том, что действие полиамина в отношении этих соединений не связано с эффектом заместительной терапии. Хотя содержание серина под действием таурина и не достигало контрольных значений, тем не менее уровень этаноламина уже в середине лечения нормализовался, чего не удавалось достичь к концу лечения с применением полиамина.
Таурин не оказал влияния на содержание в плазме крови метионина, однако нормализовал концентрацию цистина. Таким образом, повышение содержания метионина на фоне остающегося низким уровня цистина после введения полиамина является эффектом заместительной терапии [Терехов Н.Т., 1984] и не ликвидирует нарушение метаболизма серусодержащих аминокислот. Таурин, наоборот, очевидно, способен включать цепь метаболических превращений метионина. Ускорение потока серусодержащих аминокислот можно считать весьма вероятным, учитывая также тенденцию к увеличению концентрации непосредственного предшественника таурина - цистеиновой кислоты.
После одновременного применения таурина и полиамина изменения в фонде серусодержащих аминокислот были сходны с таковыми после применения таурина, однако повышался также уровень метионина, а уровень цистеиновой кислоты к моменту выписки был достоверно выше, чем при поступлении. Это может свидетельствовать о вовлечении введенного извне метионина в дальнейшие метаболические превращения, в том числе, возможно, в реакциях трансметилирования за счет ускорения потока S-аденозилметионина [Chawla R.K., 1990]. Остальные сдвиги были однонаправленными с таковыми после введения полиамина, однако содержание аланина достигало контрольных значений.
Таким образом, совместное применение таурина и полиамина способно оказать корригирующее влияние на все основные звенья аминокислотного дисбаланса при ОАСНК: достичь адекватной коррекции метаболизма серусодержащих аминокислот и более полного восстановления уроней гликогенных аминокислот. Кроме этого, эффекты полиамина и таурина в отношении исследуемых соединений можно считать суммирующимся, что хорошо заметно па примере этаноламина. Восстановление как уровней, так и метаболических соотношений в обмене серусодержащих аминокислот следует считать основным эффектом, метаболически обосновывающим рациональность совместного применения полиамина и таурина.
При наличии сопутствующей язвенной болезни желудка и 12-перстной кишки у больных ОАСНК II стадии, при традиционной терапии проявления аминокислотного дисбаланса не устранялись, причем концентрации треонина, глицина, глутамина и лизина к моменту выписки достоверно снижались по отношению к контролю, что позволяет говорить об усугублении явлений метаболического дисбаланса. Концентрации треонина, аланина, валина, метионина, глицина, изолейцина, тирозина и фенилаланина, которые при поступлении были ниже контрольных значений, нормализовались к концу лечения. Концентрации этаноламина и гистидина оставались ниже контрольных значений. Наконец, полиамин не оказал влияния на уровни серусодержащих аминокислот, кроме цистина. Последний, хотя и достоверно повышался к концу лечения, однако оставался в 2 раза ниже контрольных значений. Таким образом, значительная часть проявлений аминокислотного дисбаланса при ОАСНК II ст. с сопутствующей язвенной болезнью после применения полиамина устраняется или имеет явную тенденцию к уменьшению.Однако, препарат не полностью устранял снижение уровней гликогенных аминокислот и функциональный дефицит серусодержащих аминокислот, а также соединений, обладающих свойствами эндогенных антиоксидантов. Полиамин практически полностью нормализовал концентрации большинства незаменимых аминокислот, однако был неэффективен для ликвидации функционального дефицита таурина.
Применение таурина у этих больных на фоне традиционной терапии ОАСНК приводило к повышению уровней аспарагина и глутамина, хотя они и не достигали контрольных значений. Влияние таурина на концентрацию аланина было аналогичным влиянию полиамина, что может свидетельствовать о том, что действие полиамина в отношении этих соединений не связано с эффектом заместительной терапии. Хотя содержание серина под действием таурина не изменялось, уровень этаноламина полностью нормализовался. Сдвиги в уровнях серусодержащих аминокислот после применения таурина изменялись так же, как и у больных без сопутствующей язвенной болезни.
Восстановление как уровней, так и метаболических соотношений в обмене серусодержащих аминокислот следует считать основным эффектом, метаболически обосновывающим рациональность применения таурина, однако применение полиамина у этой категории больных не менее оправдвно, исходя из нормализующего эффекта препарата в отношении фонда незаменимых аминокислот, восстановление которого у этих больных особенно актуально [Терехов Н.Т., 1984].
У больных, перенесших резекцию желудка по Бильрот-II по поводу язвенной болезни, после традиционной терапии практически не наблюдалось положительной динамики в фонде свободных аминокислот и их производных в плазме крови. Исчезало только снижение уровней лизина и цистеата. На фоне применения полиамина происходила нормализация уровней большинства незаменимых аминокислот (треонин, валин, изолейцин, лейцин), а также аспартата, серина, глицина и аланина. Содержание аспарагина и цистина повышалось, но не достигало контрольных значений, а глутамата и глутамина - не изменялось. Таким образом, полиамин оказался способным нормализовать ряд метаболических сдвигов у больных ОАСНК, перенесших резекцию желудка. Однако, как и у других больных ОАСНК, полиамин практически не влиял на пул серусодержащих аминокислот. Так как изменения в спектре серусодержащих аминокислот у этой группы больных были наиболее глубокими и соответствовали наблюдавшимся при IV стадии заболевания, коррекция их весьма актуальна и назначение таурина этим больным следует считать необходимым. Количество наших наблюдений (3) недостаточно для репрезентативной клинической группы, однако у всех этих больных концентрации таурина и цистеиновой кислоты к концу лечения находилась в пределах средней ошибки контрольной группы. Как и в предыдущем случае, назначение таурина этим больным должно сопровождаться парентеральным введением аминокислотных смесей для коррекции изменений в фонде незаменимых (в первую очередь - АРУЦ) и гликогенных аминокислот.
При наличии сопутствующего сахарного диабета после традиционной терапии ОАСНК аминокислотный дисбаланс не устранялся. Характер сдвигов в формировании аминокислотного фонда был практически таким же, как при поступлении: абсолютный дефицит таурина, АРУЦ и гликогенных аминокислот. К моменту выписки после традиционного лечения повышался уровень пролина выше контрольных значений, достоверно повышался уровень глутамина, однако, оставался более чем в 3 раза ниже контрольных значений.
Оказалось, что дополнительное включение Тау в схему лечения больных способствует нормализации уровня глюкозы в крови (5,34±0,71 ммоль/л). Кроме этого, назначение Тау способствует ликвидации существующего аминокислотного дисбаланса в физиологических жидкостях больных. Так, концентрация таурина после его применения была близка к контрольным цифрам, одновременно восстанавливались концентрации метионина и цистина, что позволяет говорить о нормализующем эффекте препарата на фонд серусодержащих аминокислот. Повышались концентрации аспарагина и глутамина, хотя последняя оставалась достоверно ниже контроля. Таурин обладал нормализующим эффектом в отношении АРУЦ и гликогенных аминокислот, хотя при примененной дозе и режиме введения этот эффект был недостаточным.
Применение полиамина в данном случае, хотя и не устраняло дефицита таурина, однако приводило к повышению содержания цистина и нормализации содержания метионина. Таким образом, полиамин оказывал определенный эффект в отношении дисбаланса серусодержащих аминокислот.
После применения полиамина содержание глутамата оставалось повышенным, а этаноламина - сниженным. Концентрации остальных соединений, которые были снижены при поступлении больных, к концу лечения достоверно повышались, включая глутамин и аспарагин. Приходили к контрольным значениям концентрации АРУЦ, глицина, серина и аланина. Таким образом, полиамин при его применении у больных ОАСНК на фоне сахарного диабета оказался способен существенно уменьшить или устранить проявления аминокислотного дисбаланса, хотя не устранял имеющийся у этих больных абсолютный дефицит таурина. Как таурин, так и полиамин не нормализовали концентрацию в плазме крови этаноламина. Вероятно, было бы целесообразно применение у таких больным аминокислотных смесей, содержащих таурин, а также глутамин [Smith R.J., 1990].
Нами у 15 человек с диабетической стопой и на фоне ОАСНК выполнена экономная ампутация гангренозно измененных пальцев и некротических участков стопы с применением вапоризации некротических тканей расфокусированным лучом СО2-лазера и одновременно свободной аутодермопластикой расщепленным кожным лоскутом, когда было невозможно наложить первичные или вторичные отсроченные швы. Всем этим больным для коррекции имеющегося аминокислотного дисбаланса, в дополнение к традиционному лечению сахарного диабета и атеросклероза, назначались таурин и полиамин. У всех больных нам удалось избежать высоких ампутаций конечностей, несмотря на то, что у некоторых больных в связи с диабетической нейро-, а также макро- и микроангиопатиями отмечались тяжелые гнойно-некротические осложнения (флегмоны стопы, гнойные тендовагиниты и т.д.).
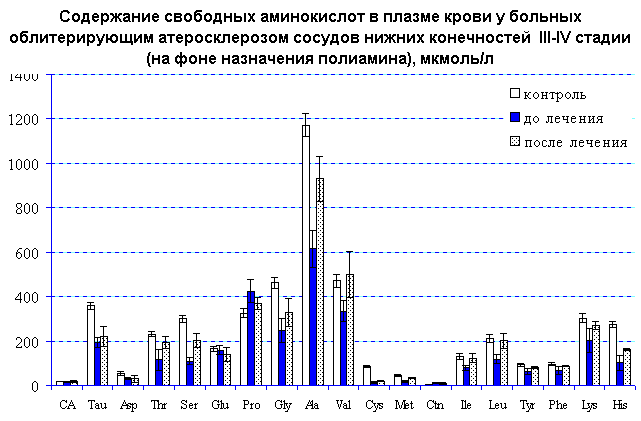
У 30 больных облитерирующим атеросклерозом ног III-IV стадии для коррекции аминокислотного баланса и метаболизма в целом на фоне традиционного лечения нами назначалась искусственная смесь для перорального питания Тонус-1, обогащённая таурином (15г? 3 раза в день, 21 день). Мы выбрали такой способ применения, учитывая, что при поздних стадиях заболевания аминокислотный дисбаланс характеризуется выраженным дефицитом серусодержащих аминокислот, что требует длительного применения препаратов, способных оказывать корригирующее воздействие. В этих условиях оправдано обогащение таурином диеты и использование таурина в качестве пищевой добавки [Geggal H.S., 1985]. Второй группе больных ОАСНК III-IV ст. назначался полиамин (15 больных).
После применения полиамина в плазме крови больных уже в середине лечения повышалось содержание серотонина. Содержание катехоламинов и кислых метаболитов дофамина не изменялось. Таким образом, полиамин при применении у больных ОАСНК III-IV стадий был менее эффективен в отношении нормализации уровней биогенных аминов, чем при II стадии заболевания. Кроме этого, нам не удалось продемонстрировать связь повышения со держания серотонина с уровнем предшественника.
Таурин при его назначении в составе питательной смеси "Тонус-1" также вызывал повышение содержания серотонина в плазме крови и повышал содержание гомованилиновой кислоты и норадреналина. Последнее приводило к нормализации соотношения норадреналина и адреналина. Таким образом, эффекты таурина в отношении пула биогенных аминов и родственных соединений были однонаправленными с таковыми у больных ОАСНК II ст. Это доказывает возможность получения эффектов этого соединения при его назначении в качестве пищевой добавки, т.е. в более низких дозах, чем при его применении в качестве лекарственного препарата.
После традиционного лечения у больных III и IV стадий проявления аминокислотного дисбаланса и его направленность не устраняются, из чего следует необходимость прямой коррекции сдвигов в содержании свободных аминокислот и их производных при поздних стадиях заболевания.
Применение полиамина у больных ОАСНК III-IV ст. приводило к нормализации концентраций треонина, валина, лейцина, изолейцина, фенилаланина и тирозина, а также лизина. Повышались по сравнению с величинами при поступлении уровни серина, метионина и гистидина. Таким образом, применение полиамина у этих больных было эффективным, однако в отношении ряда показателей не было достигнуто эффекта нормализации, как у больных II стадии. Сохранялся дефицит гликогенных аминокислот. Кроме этого, полиамин не устранял недостаточности таурина и не ликвидировал других сдвигов в обмене серусодержащих аминокислот, кроме метионина. Эффекты полиамина в отношении серусодержащих аминокислот не выходят за рамки заместительной терапии.
Назначение питательной смеси "Тонус -1" на фоне традиционной терапии больных ОАСНК III-IV стадии приводило к нормализации уровней серусодержащих, гликогенных аминокислот, а также АРУЦ, что свидетельствует об активации процессов синтеза и транспорта серусодержащих соединений, глюконеогенеза. Концентрации ароматических аминокислот оставались сниженными. Основным результатом применения таурина в виде компонента лечебного питания является достигнутая нами коррекция фонда серусодержащих аминокислот, практически аналогичная таковой после курсового применения таурина в таблетированной форме, а также тенденция к нормализации содержания гликогенных аминокислот и АРУЦ.
Таким образом, полученные результаты обосновывают целесообразность включения питательной смеси "Тонус-1", обогащенной таурином в схему лечения больных облитерирующим атеросклерозом сосудов нижних конечностей в III-IV стадии заболевания.
Рис.1
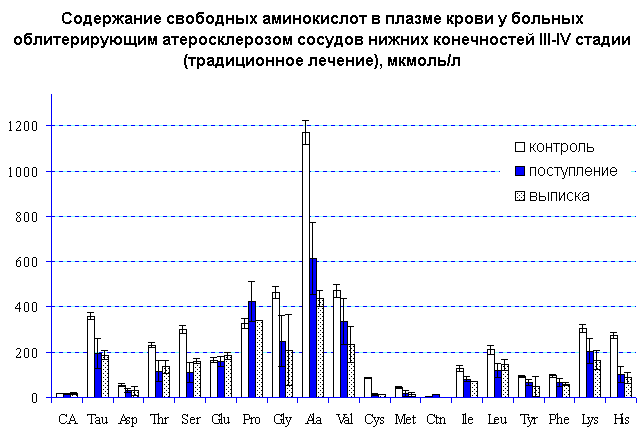
Рис.2
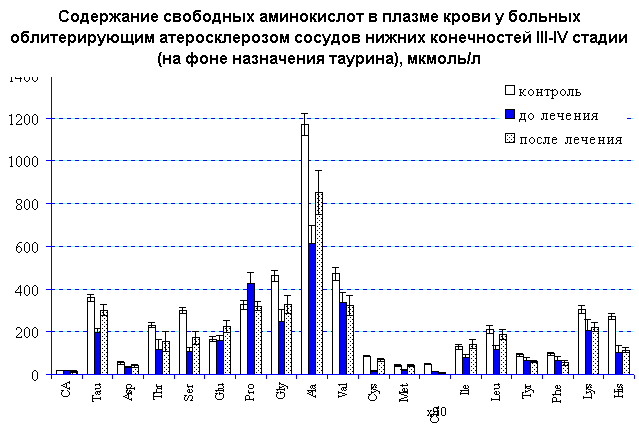
Рис.3
ВЫВОДЫ
1. Изменения в уровнях свободных аминокислот и их производных достаточно специфичны и информативны для диагностики, эффективности лечения и оптимизации способов метаболической коррекции облитерирующего атеросклероза сосудов нижних конечностей.
2. Повышение концентрации таурина , вызванное его экзогенным введением, активирует транспорт аминокислот из кровяного русла в ткани, процессы утилизации их углеродных радикалов в ЦТК и деградацию серусодержащих аминокислот, а также оказывает антиоксидантное действие, что метаболически обосновывает применение таурина в качестве антиатерогенного средства.
3. Таурин оказывает адаптогенное действие на процессы формирования фонда свободных аминокислот и метаболически связанных с ними соединений (биогенные амины) при экспериментальном атеросклерозе. Применение таури в экспериментальной модели атеросклероза у крыс и кроликов вызывает патоморфологическую и биохимическую регрессию присущих данной патологии признаков и эффективно с позиций его нормализующего действия на пул серусодержащих, гликогенных аминокислот и восстановление нормального соотношения АРУЦ и ароматических аминокислот в печени и плазме крови. Применение таурина представляется с метаболических позиций наиболее рациональным для ликвидации существующего при атеросклерозе метаболического дисбаланса.
4. Облитерирующий атеросклероз сосудов нижних конечностей характеризуется выраженным аминокислотным дисбалансом, главным образом за счет изменения уровня гликогенных и серусодержащих аминокислот, выраженность которого зависит от стадии заболевания. Существующие традиционные методы лечения исследуемой патологии не приводят к ликвидации аминокислотного дисбаланса. Уже у больных I стадии имеется ряд сдвигов в содержании биогенных аминов, их предшественников и метаболитов в плазме крови, которые не устраняется полностью при традиционном лечении.
5. Назначение при консервативном
и хирургическом лечении ОАСНК (в пред- и послеоперационном периоде) искусственных
смесей аминокислот и таурина способствует ликвидации существующего аминокислотного
дисбаланса в плазме крови больных, а также нормализации клинико-биохимических
показателей, улучшает результаты лечения больных ОАСНК, способствуя улучшению
объективного статуса, сокращению сроков пребывания больных в стационаре
и снижению процента ампутации конечностей.
ЛИТЕРАТУРА
SUMMARY
The formation of the amino acid pool in blood plasma and tissues of rats with experimental atherosclerosis has been investigated. The anti-atherogenic activities of taurine under above conditions has been demonstrated.
It was shown that the patients with obliterating atherosclerosis of lower limbs is accompanied with amino acid imbalance. The shifts in the levels of free amino acids are specific and informative for the prognosis and must be taken into account in choosing the scheme of metabolic correction in the above pathology.
With liver and blood plasma taurine concentrations being increased, which was induced by its single i.p. administration at a dose of 0.1LD50 (650 mg/kg), we demonstrated the antiradical and antioxidative activities of this compound (inhibition of Fe2+-induced chemoluminescence). The liver showed increased concentrations of general phospholipids, phosphatidylcholine and sphingophosphatides, the levels of ethanolamine, glutamate, methionine and cysteic acids were decreased, while the concentrations of phosphoethanolamine, reduced glutathione and CoASH raised and mitochondrial cysteine decarboxylase and cysteine transaminase activated. The activities of mitochondrial pyruvate and 2-oxoglutarate dehydrogenase which regulate tricarboxylic acid cycle functions as well as the 2-oxoglutarate level and NAD+/NADH ratio were elevated, whereas the acetyl-CoA/CoASH ratio diminished, which indicates an enhanced carbon flow into the tricarboxylic acid cycle. All the above enables us to recommend Tau an antiatherogenic remedy.
Taurine possesses an adaptogenic properties in relation to the formation of the pool of free amino acids and related compounds in experimental atherosclerosis.
A relative deficiency of glucogenic and sulfur-containing amino acids can be observed in all patients with obliterating atherosclerosis of the lower limbs. The severity of the amino acid imbalance depends on the stage of the disease. Traditional therapy of atherosclerosis does not eliminate the symptoms of the amino acid imbalance.
Administration of taurine and amino acid solutions as a supplement to the traditional conservative and operative treatment of athersclerosis can result in the elimination of the metabolic imbalance and reduction of the thrombotic complications.
Fifteen patients with diabetic foot combined with diabetic atherosclerosis underwent economic amputation of gangrenously changed toes and necrotic parts of the foot using vaporization of the necrotic tissues by an unfocused beam of a CO2-laser and free autodermoplastics, when it was impossible to place the primary or secondary delayed sutures. To correct not only the carbohydrate metabolism but also the amino acid imbalance, all patients received taurine and polyamine as supplements to conventional treatment. We managed to avoid high amputations in spite of the fact that some patients due to diabetic neuro-, micro- and macropathies had severe pyo-necrotic complications.
The supplementary application of taurine (0,5, 3 times a day) and polyamine (400 ml, ten times, in a day) not only eliminated the blood amino acid imbalance but also normalized the level of blood glucose, thus improving the objective status, decreasing the period of inpatient treatment and reducing the percentage of high amputations.
To improve the results of treatment of patients with obliterating atherosclerosis of the lower extremities by a purposeful correction of the amino acid imbalance, we used the taurine-containing nutritional mixture Tonus-1 at the steps of conservative and surgical treatment of 30 patients with obliterating atheroslerosis of the lower extremities of Stages III and IV (15 g, 3 times a day, 21 days). The pool of blood plasma amino acids and derivatives was studied. On admission of the patients to hospital the blood plasma was found to show a pronounced amino acid imbalance manifested by decreased concentrations of taurine and thiol-containing amino acids, its biosynthetic precursors, as well as glycogenic amino acids. The above changes in the blood plasma amino acid pool suggest inhibited reactions of thiol-containing amino acid biosynthesis and disturbed processes of intermediate metabolism and transport of these compounds to tissues. These alterations in the pool of free amino acids and derivatives are not eliminated by using conventional treatment and are essentially retained on discharge from the hospital. The supplementation with the nutritional mixture Tonus-1 in combination with conventional treatment abolished the existing blood plasma amino acid imbalance and tended to normalize the levels of thiol-containing, glycogenic amino acids as well as branched-chain amino acids (isoleucine, leucine, valine). The concentrations of aromatic amino acids (tyrosine and phenylalanine were considerably decreased, indicating an improved antitoxic liver function. The above improvements substantiate the advantage of the incorporation of the nutritional mixture Tonus-1 into the treatment scheme of patients with the III and IV stages of obliterating atherosclerosis of the lower extremities.