Формирование аминокислотного пула в ситуации экспериментального атеросклероза у кроликов
И.И.Климович, Е.М.Дорошенко
Гродненский Государственный медицинский институт МЗ Республики Беларусь, 230015, Гродно, Горького 80
Институт биохимии НАН Беларуси, г. Гродно, 230009, Гродно, БЛК 50
Abstract
I.I. Klimovich, Ye.M.Doroshenko. The formation of amino acid pool under conditions of experimental atherosclerosis in rabbits
Key words: atherosclerosis, amino acids, taurine, animal models
The formation of the amino acid pool in blood plasma and tissues of rabbits with experimental atherosclerosis has been investigated.
Experimental atherosclerosis in rabbits can be characterized by amino acid imbalance in blood plasma and tissues which includes decrease of the ratio of branched-chain amino acids to aromatic ones, deficiency of glucogenic amino acids (serine, glycine) and decrease of the concentration of glutamate. The deficiency of taurine which was not mediated through the precursor alailability was demonstrated in blood plasma; absolute taurine deficiency took place in all tissues studied. The mechanisms of the development of the taurine deficiency might include an inhibition of metabolic conversions of methionine (in all tissues studied), shifts in the relative significance of the ways of degradation of cysteine (in heart), and decrease of decarboxylation of cysteic acid (in the liver and probably in the muscles). Any of the above mechanisms as well as their combination make us consider the methionine administration in atherosclerosis to have no metabolic reason.
Введение
Изучению закономерностей формирования фонда свободных аминокислот и их производных, а также метаболических процессов, определяющих эти явления, посвящены лишь единичные работы. Однако, исследование этих закономерностей является актуальным, так как, во-первых, установлено, что первичным при атеросклерозе является нарушение не липидного, а белкового обмена [1]. Во-вторых, аминокислоты являются наиболее важными соединениями, участвующими в синтезе большинства эндогенных биологически активных соединений, в том числе аллостерических регуляторов, нейротрансмиттеров или их предшественников [2,3,4]. В патогенезе атеросклеротических окклюзионных заболеваний существенное значение имеют агрегация тромбоцитов и тромбирование артерий [5]. В механизмах указанных процессов принадлежит ведущая роль биологически активным соединениям эндогенного происхождения, в первую очередь, - нейроактивным соединениям - аминокислотам и их производным - биогенным аминам. Их роль в регуляции сосудистого тонуса, активности реакций утилизации липидов, всасывания и утилизации холестерина не вызывает сомнений [6]. Нарушения структуры эндотелия, морфологически определяемые в долипидной стадии атеросклероза, могут быть связаны и с нарушением функции тромбоцитов [7,8].
В профилактике и лечении атеросклероза и его осложнений одно из ведущих мест отводится антиоксидантам природного происхождения [1]. Известно, что к последним в первую очередь относятся серусодержащие аминокислоты и их дериваты [9,10,11,12]. Доказано, что избыточное введение серусодержащих аминокислот с пищей способно повысить уровень глутатиона в печени крыс [13]. В связи с этим актуальным является исследование механизмов реализации биологической активности и формирования внутриклеточного фонда важнейшего продукта деградации серусодержащих аминокислот - таурина (Тау) [10,12,14,15,16]. Так, показано, что при введении Тау in vivo он оказывает гиполипидемическое и гипохолестеринемическое действие [17], активирует реакции всасывания и утилизации липидов и холестерина [12,18,19]. Кроме того, нейромодуляторные свойства и высокие концентрации Тау в тромбоцитах [17] определяют его участие в процессах агрегации, тромбирования артерий и регуляции сосудистого тонуса.
С целью исследования формирования фонда свободных аминокислот плазмы крови и периферических тканей нами воспроизведена модель экспериментального атеросклероза у кроликов. Моделирование атеросклероза на кроликах [20] позволяет вызвать макроскопические изменения со стороны крупных артерий, вызывающие нарушения регионарного кровотока, следовательно, и те метаболлические нарушения, которые являются следствием хронической гипоксии тканей, а не только самого атеросклероза как системной (обменной) патологии. Именно такой (комбинированный) характер метаболических расстройств наиболее вероятно наблюдать в клинических условиях [21], так как все клинические проявления атеросклероза проявляются при появлении ишемических расстройств, которые возможны при наличии макроскопически определяемых поражений сосудов.
Материалы и методы
В опытах использовались и кролики-шиншила, полученные из питомника РАМН "Рапполово" и содержавшиеся на стандартном рационе вивария со свободным доступом к воде. Экспериментальная модель атеросклероза реализована на 20 кроликах-шиншила при содержании животных в течение двух месяцев на рационе, в состав которого, наряду со всеми необходимыми компонентами, входили 10% холестерина, 30% говяжего жира и 0,005% мерказолила [20].
В работе использовали: стандарты аминокислот и их производные фирм Fluka, Serva, Sigma, Reanal; остальные реактивы - фирмы "LaChema" (Чехия). Стандартные растворы аминокислот производства фирм "Calbiochem" и "Fluka AG". Органические растворители имели квалификацию "для жидкостной хроматографии". Экстракционные среды и подвижные фазы, а также растворы стандартов готовили с использованием воды для ВЭЖХ, полученной тройной дистилляцией в стеклянном аппарате с последующим пропусканием через патрон "Norganic" и фильтрованием через мембранный фильтр HATF 0,45 мкм (Millipore, США) [22].
Кровь отбиралась в гепаринизированные пробирки. Образцы периферических тканей (печени, скелетной мышцы, миокарда) забирали в течение 1 мин после забоя и фиксировали в жидком азоте. Плазму получали путем центрифугирования крови в течение 15 минут при 1500 об/мин. Для депротеинизации к 0,5 мл плазмы добавляли равный объем 1M НСlО4 (в качестве внутреннего стандарта в нее добавляли норлейцин из расчета 1250 нмоль/мл) и центрифугировали в течение 15 минут при 8000 об/мин. После этого для нейтрализации добавляли цитратный буфер (57 г водного цитрата Li х 4H2O, 42г лимонной кислоты х H2O на 200 мл раствора) из расчета 150 m л на 1мл полученного образца [23].
Образцы печени, сердца и мышечной ткани, до исследования хранившиеся в жидком азоте, гомогенизировались при 800 об/мин в гомогенизаторе со стеклянным пестиком в 10 объемах 0,2М HClO4, с добавлением внутреннего стандарта (n-Leu) из расчета 12,5 m М/г ткани. После этого полученный безбелковый экстракт отделяли от осадка. Полученные таким образом безбелковые экстракты для определения фонда свободных аминокислот хранилось в течение всего времени до анализа при температуре -20°С [23,24].
Количественная и качественная идентификация свободных аминокислот и их дериватов проводилась катионообменной хроматографией одноколоночным методом на автоанализаторе аминокислот Т-339 (ЧСФР) по модифицированному методу Benson J.V., Paterson J.A. [24].
Принцип метода заключается в элюции аминокислот и родственных им соединений ступенчатым градиентом Li-цитратных буферных растворов [25]. После нанесения кислотного экстракта физиологических жидкостей или тканей на аналитическую колонку (22,0 х 0,35 см), заполненную сферическим катионообменником LGAN 2B (размер частиц 8 мкм) ("Lachema", Чехия) хроматографическое разделение исследуемых соединений последовательно осуществлялось Li-цитратными буферами. Скорость потока растворов 14 мл/час. Температура анализа дискретно повышалась в середине аналитического цикла с 40 до 62°С. Количественное содержание каждого компонента спектра исследуемых соединений оценивалось по реакции с 1% раствором нингидрина (скорость потока 12 мл/час) в капиллярной бане при 100°С при длине волны 520 нм после прохождения через проточную кювету однолучевого фотометра [11,23]. Прием и обработка хроматографических данных осуществлялась с помощью программно-аппаратного комплекса "МультиХром-1" (а/о "МультиХром", г.Москва; версия программного обеспечения - 2.67).
Качественная идентификация и количественная оценка полученных значений производилась программой путем сравнения результатов анализа исследуемых биологических объектов со стандартной калибровочной кривой искусственной смеси аминокислот и нингидринположительных компонентов. Последняя содержала равные количества определяемых соединений по 250 нмоль/мл каждого и в качестве внутреннего стандарта в нее добавляли в той же концентрации норлейцин (концентраты стандартных смесей фирмы "Calbiohem", США). В описанной системе последовательно элюировались и определены следующие соединения: цистеиновая кислота (CA), таурин (Tau), фосфоэтаноламин (PEA), мочевина (urea), аспарагиновая кислота (Asp), ОН-пролин (H-Pro), треонин (Thr), серин (Ser), аспарагин (Asn), глутаминовая кислота (Glu), глутамин (Gln), a -аминоадипиновая кислота (a -AAA), пролин (Pro), глицин (Gly), аланин (Ala), a -аминомасляная кислота (a -ABA), цитруллин (Ctr), валин (Val), цистин (Cys), метионин (Met), цистатионин (Ctn), изолейцин (Ile), лейцин (Leu), норлейцин (n-Leu), b -аланин (b -Ala), b -аминомасляная кислота (b -ABA), g -аминомасляная кислота (GABA), этаноламин (EA), аммиак (NH3), орнитин (Orn), лизин (Lys) и гистидин (His). Средние значения показателей в группах сравнивали с помощью Т-критерия Стьюдента с помощью программы 3d из пакета ВМDР (BMDP Statistical Software).
Результаты и обсуждение
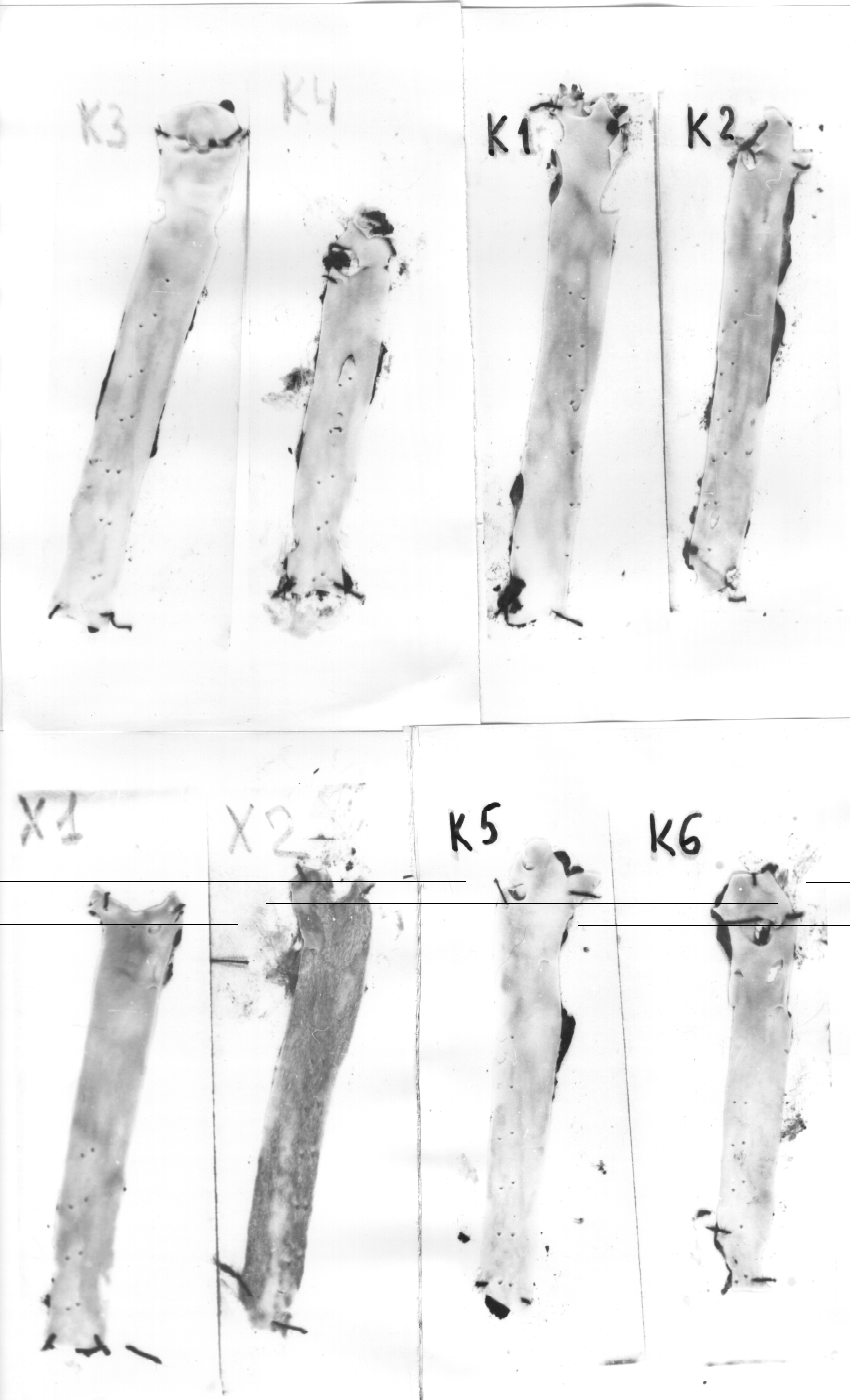
При макроскопическом исследовании аорты животных опытной группы обнаружено: внутренняя поверхность аорты неровная за счет выступающих в просвет атеросклеротических бляшек и полосок с локализацией в области дуги, восходящем отделе аорты, в грудном отделе и брюшной части аорты в местах отхождений крупных кровеносных сосудов. Дефектов интимы и тромботических наложений не обнаружено (рис.1).

Рис.1. Макроскопическая картина аорты животных опытной группы (X1 и X2) и контрольной группы (К5 и К6).
Микроскопическая картина аорты в области локализации атеросклеротических бляшек у всех животных опытной группы имела однотипный характер: интима утолщена, особенно по краям липидной линзы. Липиды при окраске суданом черным В выявлялись в ксантомных клетках, а также экстрацеллюлярно. В области бляшек наблюдалась деструкция эластических волокон и разрастание соединительной ткани. Явлений атероматоза у экспериментальных животных не обнаружено.
Таким образом, в данном эксперименте удалось воспроизвести неосложненное атеросклеротическое поражение аорты с выраженной картиной липоидоза [20].
Определение содержания свободных аминокислот и их производных в плазме крови и тканях кроликов в ситуации экспериментального атеросклероза позволило нам выявить наличие у них выраженного аминокислотного дисбаланса (табл. 1-4). Так, в плазме крови животных опытной группы отмечалось достоверное снижение содержания таурина, а также цистина, серина, аспартата, глутамина, валина, лейцина и этаноламина (табл. 1). Это свидетельствует о дефиците серусодержащих аминокислот, не опосредованном снижением уровня предшественника [26]. Снижение соотношения АРУЦ и ароматических аминокислот, возможно, является признаком снижения антитоксической функции печени. Дефицит серина и продукта его декарбоксилирования этаноламина может означать снижение антиоксидантной защиты [27]. Таким образом, при экспериментальном атеросклерозе у кроликов наблюдается явный дефицит таурина. Вероятно, введение метионина в данной ситуации не будет эффективным, так как содержание цистина было значительно снижено при нормальном уровне метионина, т.е. возможно, метаболический блок существует на уровне SAM-синтазы или реакций трансметилирования [28].
В печени животных опытной группы также отчетливо выявлялся дефицит таурина, при этом содержание метионина и цистеиновой кислоты было выше контрольных значений, а цистина - снижено (табл. 2). Это, с одной стороны, подтверждает предположение о наличии ингибирования реакций синтеза цистеина [29], а с другой стороны, позволяет предположить также увеличенный расход таурина в реакциях конъюгации [30] либо торможение декарбоксилирования цистеата [31]. Последнее более вероятно, учитывая низкий уровень цистина. Таким образом, снижение синтеза таурина при экспериментальном атеросклерозе, очевидно, не обусловлено изменением соотношения между двумя путями превращений цистеина - окислением и переаминированием [32].
Как и в плазме крови, в ткани печени была снижена концентрация этаноламина, но это снижение не было обусловлено уровнем предшественника. Это позволяет предположить снижение антиоксидантных функций в печени (что дополнительно подтверждается низкой концентрацией цистина) [33]. Соотношение между концентрациями АРУЦ и ароматических аминокислот в печени изменялось однонаправленно с таковым в плазме крови, однако его механизмом в данном случае было повышение уровня ароматических аминокислот (тирозина).
В сердечной мышце обнаружено существенное снижение содержания таурина (более чем в 3 раза) на фоне сниженного содержания как цистина, так и цистеата (табл. 3). Снижалось также содержание мочевины, глутамата, глутамина, гистидина и серина. Снижение содержания этаноламина здесь не было статистически достоверным. Таким образом, дефицит таурина в сердечной мышце может быть обусловлен как снижением синтеза цистеина, так и перераспределением путей его превращений. Имеет место также выраженный дефицит гликогенных аминокислот.
Наконец, в скелетных мышцах кроликов имело место снижение содержания таурина на фоне неизменных концентраций цистина и цистеиновой кислоты и повышенной концентрации метионина (табл. 4). Кроме этого, повышалось содержание аммиака, тирозина и снижалось - серина. Повышение концентрации аммиака можно, предположительно, связать с усилением протеолиза и деградации свободных аминокислот, учитывая отсутствие общего обогащения пула, характерного для активации протеолиза [34].
Таким образом, в ситуации экспериментального атеросклероза у кроликов во всех исследованных тканях и плазме крови выявлен абсолютный дефицит таурина, механизмами развития которого могут быть торможение активности SAM-синтазы, перераспределение путей деградации цистеина в пользу его переаминирования, а также угнетение декарбоксилирования цистеата. Любой из этих механизмов, как и их сочетание, позволяет считать назначение метионина в данной ситуации метаболически необоснованным, так как основным нарушением в обмене серусодержащих аминокислот является дефицит таурина, который в данной метаболической ситуации не будет эффективно устраняться применением метионина, особенно, учитывая адаптационные сдвиги активностей ферментов метаболизма серусодержащих аминокислот к избытку метионина [35]. Кроме этого, более или менее постоянно наблюдалось снижение содержания в тканях глутамина, что может объясняться нарушением его синтеза в печени [36] а также серина и/или этаноламина.
Таблица 1
Содержание свободных аминокислот и их производных в плазме крови кроликов при экспериментальном атеросклерозе, m М
|
n=6 |
n=13 |
|
| CA |
|
|
| Tau |
|
|
| urea |
|
|
| Asp |
|
|
| Thr |
|
|
| Ser |
|
|
| Asn |
|
|
| Glu |
|
|
| Gln |
|
|
| Pro |
|
|
| Gly |
|
|
| Ala |
|
|
| aAba |
|
|
| Val |
|
|
| Cys |
|
|
| Met |
|
|
| Ctn |
|
|
| Ile |
|
|
| Leu |
|
|
| Tyr |
|
|
| Phe |
|
|
| bAla |
|
|
| EA |
|
|
| NH3 |
|
|
| Orn |
|
|
| Lys |
|
|
| His |
|
|
*: p<0.05 при сравнении с контролем
Ранее был исследован фонд свободных аминокислот и их производных в миокарде в динамике поступления Тау в фармакологически активных дозах. Для этого он вводился крысам-самцам массой 140-160 г ежедневно внутрибрюшинно в дозе 1/10 LD50 (650 мг/кг массы тела) на протяжении 1, 3, 8 и 15 суток [37].
Оказалось, что на фоне повышения содержания Тау в миокарде, к 3 суткам эксперимента снижается содержание важнейших незаменимых (Lys, His) и аминокислот с разветвлённой углеводородной цепью (Leu, Val, Ile), концентрации которых определяют направленность основных (гликолиз, глюконеогенез, активность ЦТК, энергообеспечение) метаболических потоков, а к 8 суткам уменьшаются уровни предшественников Тау - серина и цистеата, регулирующих активность катаболизма серусодержащих соединений и окислительно-восстановительных процессов в сердечной мышце.
Полученные результаты свидетельствуют о влиянии экзогенного Тау на содержание исследованных соединений в миокарде и возможности реализации кардиотропных эффектов этого соединения на уровне регуляции превращений аминокислот и формирования их внутриклеточного фонда, определяющего функциональную активность сердечной мышцы.
Исходя из полученных данных, представляется целесообразным исследовать эффекты таурина при его длительном введении на фоне моделирования атеросклероза. Нарушения в формировании фонда свободных серусодержащих аминокислот играют существенную роль в развитии аминокислотного дисбаланса при экспериментальном атеросклерозе.
Таблица 2
Содержание свободных аминокислот и их производных в печени кроликов при экспериментальном атеросклерозе, m моль/г. Количество наблюдений - см. табл. 1.
|
|
|
|
| CA |
|
|
| Tau |
|
|
| PEA |
|
|
| urea |
|
|
| Asp |
|
|
| Thr |
|
|
| Ser |
|
|
| Glu |
|
|
| Gln |
|
|
| Pro |
|
|
| Gly |
|
|
| Ala |
|
|
| aAba |
|
|
| Val |
|
|
| Cys |
|
|
| Met |
|
|
| Ctn |
|
|
| Ile |
|
|
| Leu |
|
|
| Tyr |
|
|
| Phe |
|
|
| bAla |
|
|
| EA |
|
|
| NH3 |
|
|
| Orn |
|
|
| Lys |
|
|
| His |
|
|
*: p<0.05 при сравнении с контролем
Таблица 3
Содержание свободных аминокислот и их производных в сердечной мышце кроликов при экспериментальном атеросклерозе, m моль/г. Количество наблюдений - см. табл. 1.
|
|
|
|
| CA |
|
|
| Tau |
|
|
| urea |
|
|
| Asp |
|
|
| Ser |
|
|
| Thr |
|
|
| Glu |
|
|
| Gln |
|
|
| Pro |
|
|
| Gly |
|
|
| Ala |
|
|
| aAba |
|
|
| Val |
|
|
| Cys |
|
|
| Met |
|
|
| Ctn |
|
|
| Ile |
|
|
| Leu |
|
|
| Tyr |
|
|
| Phe |
|
|
| bAla |
|
|
| EA |
|
|
| NH3 |
|
|
| Orn |
|
|
| Lys |
|
|
| His |
|
|
*: p<0.05 при сравнении с контролем
Таблица 4
Содержание свободных аминокислот и их производных в мышцах кроликов при экспериментальном атеросклерозе, m моль/г. Количество наблюдений - см. табл. 1.
|
|
|
|
| CA |
|
|
| Tau |
|
|
| PEA |
|
|
| urea |
|
|
| Asp |
|
|
| Thr |
|
|
| Ser |
|
|
| Glu |
|
|
| Gln |
|
|
| Pro |
|
|
| Gly |
|
|
| Ala |
|
|
| Val |
|
|
| Cys |
|
|
| Met |
|
|
| Ctn |
|
|
| Ile |
|
|
| Leu |
|
|
| Tyr |
|
|
| Phe |
|
|
| bAla |
|
|
| EA |
|
|
| NH3 |
|
|
| Orn |
|
|
| Lys |
|
|
| His |
|
|
*: p<0.05 при сравнении с контролем
Литература
1. Репин В.С., Смирнов В.Н. Фундаментальные науки против атеросклероза -
2. Amino Acids (Chemistry, Biology, Medicine) / Ed. Lubec C., Rosental J.A. - N.Y.: Escom, 1990. - 1196 p.
3. De Feudis F.V., Mandel P. Amino Acid Neurotransmitters. - N.Y.: Acad.Press, 1981. - 571 p.
4. The role of amino acids in the brain/ Quastel J.H., Marks V., Lajtha A., et al.. - London. - N.Y.: Raven Press, 1979. - 298 p.
5. Климов А.Н., Никульчева Н.Г.. Липиды, липопротеиды и атеросклероз. СПб., 1995.- 298с.
6. Некоторые показатели тромбоцитарной активности больных облитерирующим атеросклерозом артерий нижних конечностей / Якунин Г.А., Кургузов О.П., Лаврова Л.А., Новикова А.Н. // Лаб.дело.- 1990.-№3.-С.77-78
9. Западнюк В.И., Купраш Л.П., Заика М.С. Аминокислоты в медицине. - Киев: Здоров'я, 1982. - 200с.
10. Нефёдов Л.И. Проявления биологической активности таурина (обзор) // Весцi АН Беларусi.- 1992. - №3-4. - С. 99 - 106.
11. Нефёдов Л.И. Формирование фонда свободных аминокислот и их производных в условиях метаболического дисбаланса, автореф. дисс.докт. мед. наук, Минск, 1993, 34с.
12. Amino Acids (Chemistry, Biology, Medicine) / Ed. Lubec C., Rosental J.A. - N.Y.: Escom, 1990. - 1196 p.
13. Bauman P.F., Smith T.K., Bray T.M. The effect of dietary protein and Sulfur-containing amino acids on hepatic glutathione concentration and glutathione-dependent enzyme activities in the rat // Can. J. Physiol. Pharm. - 1988. - V. 66. - P. 1048-1052.
14. Гуревич В.С. Таурин и функция возбудимых клеток. - Л.: Наука, 1986. - 108с.
15. Нефёдов Л.И. Метаболизм таурина у млекопитающих (обзор) //Весцi АН БССР. - 1990. - №5. - С. 99 - 106.
16. Hayes K., Sturman J.A. Taurine in metabolism // Ann. Rev. Nutr. - 1981. - V. 1. - P. 401.
17. Taurine: Biological Actions and Clinical Perspectives / Ed. Oia S.S., Antee L., Kontro P., et al. - N.Y.: Alan R. Liss, 1985. - 512 p.
18. Azuma J., Sawamura A., Awata N. Usefulness of taurine in chronic congestive heart failure and its prospective application // J. Circ. J. - 1992. - V.56, N.1. - P.95-99.
19. Azuma J., Halliwell B., Haey B.M. The antioxidant action of taurine, hypotaurine and their precursors // Biochem.J. - 1988. - V. 256, N1. - P.251-255.
20. Экспериментальный атеросклероз и возраст / Ред.: Н.Н.Горев // М.: Медицина, 1972.- 208с.
21. Чазов Е.И., Смирнов В.Н., Репин В.С., Ткачук В.А.. Новое в изучении патогенеза и лечении атеросклероза // Клин.медицина, 1991.- №3.- С.7-11.
22. Scott R.P.W. Liguid chromatography: past, present and future // J. Liguid Chromatogr. - 1987. - V. 10, N.8-9. - P. 1547-1569.
23. Нефедов Л.И. Хроматографические методы изучения метаболизма серусодержащих аминокислот // Теория и практика хроматографии: Тез. - Куйбышев, 1984.- С. 165.
24. New techniques in amino acid, peptide and protein analysis / ed. by A. Niederwieser and G. Pataki - Ann Arbor Sci. Publ., Inc. - 1971, 462 p.
25. Lewis J.B. Amino acid analysis: buffers and artifacts // J. Chromatogr. - 1988. - V. 436, N1. - P. 80-85.
26. Stipanuk M., Rotter M.A. Metabolism of cysteine, cysteinsulfinate and cysteinsulfonate in rats fed adequate containing amino acids // J. Nutr. - 1984. - V. 114, N8. - P. 1426-1437.
27. Быков И.Л., Тарасов Ю.А. Чумаченко С.С. Антистрессорное действие этаноламина при острой алкогольной интокикации. // Пробл. эндокринол. - 1989. - №3. - с. 72-74.
28. Букин Ю.В., Орлов Е.Н. Новые подходы к регуляции биосинтеза S-аденозилметионина и процессов трансметилирования в нормальных и злокачественных клетках. // Вест. АМН СССР. - 1984. - №5. - С. 9-14.
29. Wienstein C.L., Haschemeyer R.H., Griffith O.W. In vivo study of cysteine metabolism // J. Biol. Chem. - 1988. - V.263, N.22. - P.16568-16579.
30. Masuda M., Horisaka K. Effect of taurine and homotaurine on bile acid metabolism in dietary hyperlipidemic rats // J. Pharmacobio. - 1986. - V.9, N.11. - P.934-940.
31. Griffith O.W. Cysteinsulfinate metabolism // J. Biol. Chem. - 1983. - V. 258, N3. - P. 1591 - 1598.
32. Ishimoto Y. Transaminative pathways of cysteine metabolism in rat tissues // Physiol. Chem. - 1979. - V. 11, N1-2. - P. 189-191.
33. Влияние аминоспиртов на системы окисления лактата и этанола // Авагимян Э.А., Дурухян С.А., Гюльбаязян Т.А., Камалян Р.Г. / Биол. ж. Армения. - 1989.-Т. 40, № 10. -С. 815-819.
34. Martensson J., Larsson J., Schildt B. Metabolic effects of amino acid solutions on severely burned patients: with emphasis on sulfur amino acid metabolism and protein breakdown // J. Trauma. - 1985. - V. 25. - P. 427-432.
35. Fan D., Bas-Joyeux B., Chanez M. Adaptation of hepatic enzyme activities to methionine excess // Reprod. Nutr. Develop. - 1981. - V. 21, N4. - P. 519-529.
36. Abumrad N.N., Geer R., Blair J. Sources of hepatic Glutamine synthesis in vivo // Biol. Chem. - 1990. - V. 371. - P. 291-305.
37. Смирнов В.Ю. Фонд свободных аминокислот и их производных при избыточном поступлении таурина и его функциональной недостаточности: Автореф. дисс... к-та биологических наук. - Москва, 1998, 21 с.